
第四章 胃和小肠疾病
| 4.1 胃和小肠生理 75 | 4.5 Oddi 括约肌运动障碍 93 |
| 4.2 胃轻瘫 80 | 4.6 Oddi 括约肌关闭不全 99 |
| 4.3 慢性消化不良 84 | |
| 4.4 慢性假性肠梗阻 88 |
4.1 胃和小肠生理
一些临床综合征与胃和小肠近端运动功能异常有关,如消化不良的常见症状可能是胃运动功能紊乱的结果。
胃的动力作用如下:
・ 混合并研磨食物
・ 调节胃内容物排空到十二指肠
・ 适当时促使胃排空。
小肠动力作用如下:
・ 将食物与消化液混合
・促使消化产物与小肠的消化吸收面(粘膜)接触
・ 将废物向远端推动。
胃底和胃体上部接受摄入的食物,起储存食物的功能。
胃内压力轻度的升高,可引起胃容量增大(约300ml到1500ml)。这一适应机制,即容受性舒张,是由迷走反射所致,其可以使人短时内大量进餐成为可能。这一机制可以防止胃内压力突然升高所致的胃内容物迅速排空到十二指肠,或下段食管括约肌(lower esophageal sphincter, LES)功能不全导致胃内容物反流至食管(图4.1)。
食物的混合和研磨、胃内容物排空到十二指肠均依靠胃远端三分之二产生的蠕动收缩。这些蠕动收缩由胃起搏区(pacemaker)控制。

图4.1上端胃容受性舒张,容纳膳食和防止胃内压力突然升高。
胃起搏区
胃起搏区位于胃体大弯侧(图4.2),其产生的慢波电位是引起胃运动的基础。
每分钟3次的电去极化波,起自胃起搏区,以环形方式经胃下传到幽门和十二指肠,其叫做慢波或电控活动(electrical control activity ,ECA)(图4.3)。
不过,当峰电位与慢波叠加时,机械活动(如蠕动收缩)即起动,这可能由激素和神经刺激所致。
因为正常情况下胃内慢波机制节律为每分钟3次,因此,胃正常最大收缩频率亦为每分钟3次。
在小肠,平滑肌产生周期性变化,膜电位节律为每分钟12次。当峰电位叠加到这一慢波上并去极化达基础阈值时,小肠便发生收缩。因此,小肠正常最大收缩频率为每分钟10~12次(图4.4)。
移行运动复合波
胃和小肠的运动依人是否空腹或刚进餐而有根本的不同。
空腹期
移行运动复合波(migrating motor complex, MMC)被描述为起源于胃,经小肠向下传递的一段运动事件,是空腹期的主要模式。然而,MMC也可起自小肠的任何部位,并由此向下传递。

图4.2 胃起搏区位置。
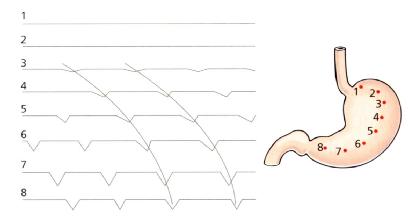
图4.3胃不同点的电活动,慢波从胃起搏区辐射。

图4.4当峰电位叠加到慢波上并去极化达基础域阈值时,小肠发生收
缩。用图经The Medicine Group (Education)有限公司许可引用。
MMC被认为有清除功能,其在两个方面可防止胃和小肠内细菌过度生长:
1 机械性地向远端移动残留物和细菌。
2 润滑(清洗)胃和小肠,因为MMC与周期性的胃酸分泌及胆汁和胰液的增加有关。
MMC在食物消化几个小时后重现(时间长短由摄入的热卡和膳食的量决定),胃开始有空心感,并开始感觉饥饿。
在白天,摄食之间的空腹期常较短(不到4小时),因此,MMC往往还没有开始,这也是MMC主要在夜间发生的重要原因。
MMC包括三个不同的运动模式(图4.5):
・ Ⅰ期:静止、无运动,持续时间为45~60分钟,此期与小肠吸收液体有关
・ Ⅱ期:幅度和频率增加的自发收缩,持续约30~45分钟,此期与胃酸(Hcl)分泌增多和小肠液增加有关
・ Ⅲ期:此期最明显,以不受干扰的一段规则收缩为特征,最大收缩率胃为每分钟3次,小肠为每分钟10~12次,持续2~12分钟。这些强力收缩使肠内容物向远端推进。
MMC的产生和演变主要由肠神经系统(肌间神经丛)负责。激素控制介导的Ⅲ期主要由胃动素来完成,不过,许多其他激素亦参与MMC的调节。
餐后
一开始进食,MMC的模式即终止,被餐后运动模式(fedmotor response)所取代,胃开始产生另一种模式的收缩(图4.6)。
在开始进食的几分钟,胃产生强蠕动收缩的稳定模式,收缩频率大约每分钟3次,以充分混合与研磨固体食物。
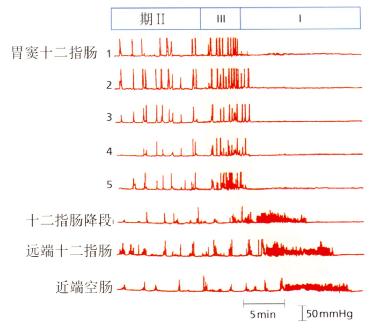
图4.5 正常空腹期活动。用图经Georg Thieme Verlag许可,引自Malagelada,1986。
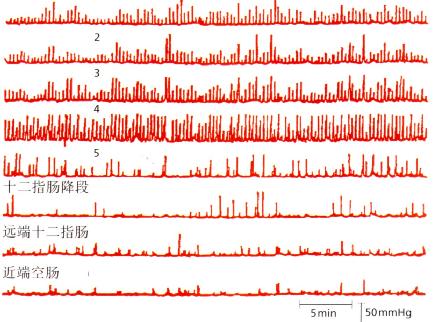
图4.6 正常进餐后(固体餐后)动力描计。用图经Georg
Thieme Verlag许可,引自Malagelada,1986。
进食后30~60分钟,在胃窦活动使固体食物排空到十二指肠之前,有一滞后期。
在小肠,食物消化导致强烈但不规则的收缩,使营养物质在肠腔内有足够的时间被消化吸收。收缩有节段性和推进性,节段性引缩增加了食物与吸收面的接触,而推进性收缩使肠内容物向远端运送。
4.2 :胃轻瘫
胃轻瘫即运动障碍引起的胃排空延迟。
胃轻瘫变化范围很大,有重度胃轻瘫(胃淤滞,即胃没有排空)和轻微的胃排空延迟。
病因
见表4.1。
症状
・ 早饱
・ 上腥烧灼感或疼痛
・ 腹胀
・ 恶心
・ 呕吐,尤其是餐后
・ 体重减轻。
鉴别诊断
・ 胃食管反流
・ 消化不良。
诊断措施
放射影像
钡餐造影可明确机械性梗阻,并且可以提示胃排空延迟的证据。然而,用该法不可能对胃排空正确定量。
表4.1 胃轻瘫的病因
| 机械性梗阻 | 胃、十二指肠溃疡疤痕形成,肿瘤 |
| 内分泌/代谢疾病 | 血糖控制不良的糖尿病酮症酸中毒、糖尿病神经病变、甲状腺功能减低,和电解质失衡K+、Ca2+) |
| 胃手术 | 迷走神经切除、部分胃切除、输出道梗阻、Roux-En-Y综合征 |
| 系统性疾病 | 硬皮病 |
| 假性梗阻 | 特发性,继发性,如肌营养不良 |
| 中枢神经系统疾病 | 脑干损伤、颅内压升高 |
| 创伤 | 头颅伤、烧伤、脊髓伤、多发伤 |
| 药物 | 抗胆碱能药、鸦片类、左旋多巴,吸毒(鸦片止痛剂) |
| 感染 | 巨细胞病毒性胃炎、病毒性胃轻瘫 |
| 特发性 | 可能与以下动力失调有关;包括胃动过速、胃窦低动力及胃十二指肠不协调 |
同位素显像
用γ照相机能测量含有固体和液体放射标记试餐的排空情况。此法为非侵入性,可以对胃排空合理和精确地定量。γ照相机检测到的敏感区的计数变化,反映了胃排空情况,连续监测能制作胃排空曲线。
然而,用放射性同位素首先应将孕妇除外,同样也不建议在同一个体反复使用。
口服药的吸收
如口服含有扑热息痛(paracetamol)的液体餐,摄取后,测定血中的扑热息痛含量。因为扑热息痛一旦排空入十二指肠即开始吸收。所以,血中随时间变化的扑热息痛含量可用作胃排空的指标。
超声
摄入液体餐后,可以用超声测量胃窦的容积,胃窦容积的减少与胃排空相关。
电阻抗
如果试餐的电传导性与周围组织不同,就可以用外置电极经腹壁测量阻抗的变化。阻抗的变化与胃排空时胃容积的减少相关。
呼吸试验
进食含有小剂量13C的辛酸(octanoic acid),可以只用呼吸分析示踪固体食物的运动。当辛酸进入十二指肠,示踪剂很快吸收且转运入肝并氧化。结果,产生的CO2呼出后可以在呼气中测到。以一定的时间间隔收集呼气样本进行分析,对胃排空进行评估。13C是稳定同位素,因此无须考虑放射衰减。
在液体食物中,用13C醋酸钠(sodium acetate)做标记物。
便携式γ计数器
先将一种对同位素敏感的胃内探头置于胃或十二指肠内,然后给患者吃放射标记的膳食,可以连续监测放射性物质在胃内被清除的过程,以确定胃排空情况见(8.9)。
胃电图
胃电图(electrogastrography,EGG)是一种可以长时间、重复记录胃电活动的非侵入性检查技术。将电极置于腹壁胃投影处(图4.7),可以记录调节蠕动的胃电节律(图4.8),EGG相对幅度和频率的变化与胃动力的变化有关(见8.8)。
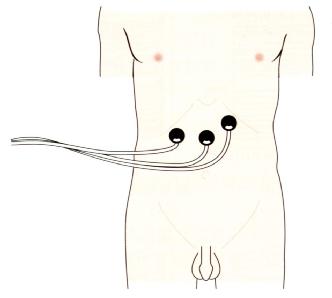
图4.7 EGG描计电极的位置。
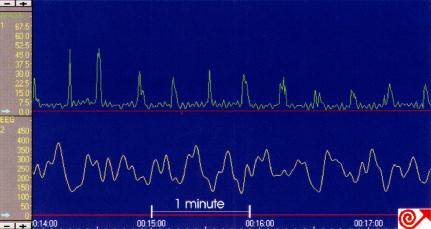
图4.8 同时行餐后EGG和胃窦测压,EGG显示每分钟3次的规则
慢波,与测压得到的每分钟3次的时相性收缩一致。
许多胃功能性紊乱有EGG模式的异常(图4.9)。
因为胃电活动是胃排空形成的主要因素之一,也就不奇怪为什么胃轻瘫的病人常可以记录到EGG节律紊乱。
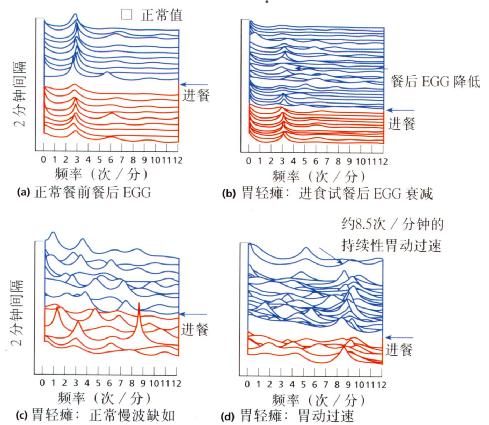
图4.9 正常情况和胃轻瘫EGG的区别。用图经American Journal
of Gastroenterology许可,引自Chen and McCallum,1992。
已有提议把EGG作为胃动力异常的筛选手段,用标准试餐后出现的频率和反应力异常作为胃运动障碍敏感和特异的指标(见8.8)。
4.3 慢性消化不良
慢性消化不良是一种常见的临床综合征,是一组排除器质性疾病后的上消化道症状。很多功能性消化不良的患者发现有消化道动力异常。
功能性消化不良依主要症状和病因分为以下亚群:
・ 反流样症候群
・ 溃疡样症候群
・ 动力异常样症候群
・ 特发性或非特异性慢性消化不良。
然而,这样分法的有效性受到怀疑,因为这些症状与动力异常并非完全相关。
病因
有许多机制用于解释消化不良症候群的发病机制。
・ 胃肠道运动功能障碍,包括:
(a)时相性收缩活动异常(食管、胃、小肠)
(b)基础状态下,消化管壁对食物、气体和液体的反应异常。
(c)胃排空延迟
・ 粘膜感染、炎症(胃炎、十二指肠球炎)
・ 胃酸分泌过多
・ 异常十二指肠胃、胃食管反流
・应激和心理因素可能起一定作用,因应激和心理因素可以改变肠道的分泌、运动和血流
・胃、十二指肠敏感性增加,功能性消化不良者,其胃扩张引起疼痛所须的胃容积较健康人要低。
症状
・ 腹痛或腹胀时间至少一个月
・ 餐后饱胀
・ 早饱或不能完成一顿正常进餐
・ 胀气
・ 恶心或呕吐
・ 呃逆
・ 烧心
・ 反食
・ 厌食。
鉴别诊断(图4.10)
・ 消化性溃疡
・ 幽门螺杆菌感染引起的胃炎
・ 胃食管反流
・ 胃肠道肿瘤
・ 肠易激综合征
・ 胆石症
・ 慢性胰腺炎
・ 胃轻瘫
・ 吞气症。
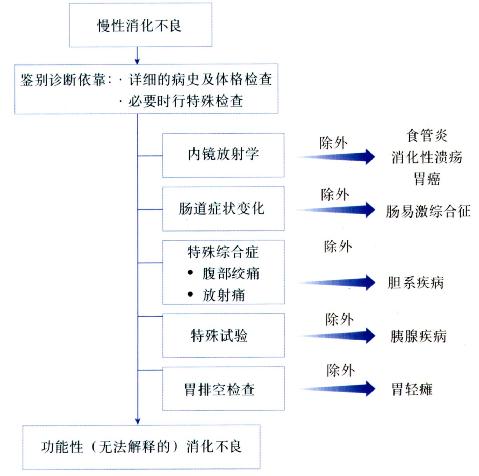
图4.10 慢性消化不良的鉴别诊断。
诊断措施
胃窦、十二指肠压力测定(图4.11)
如果内镜、放射学、pH测定等检查没有提供有力的证据,应考虑压力测定,进一步明确有无运动障碍(见8.7)。

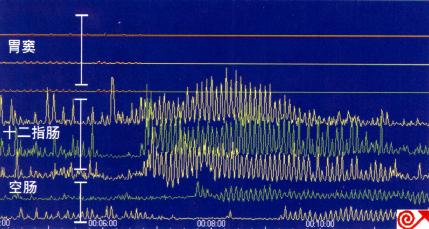
图4.11 空腹期胃窦、十二指肠压力测定。(a)非消化不良病人胃窦
通道的Ⅲ期活动。(b) 消化不良病人胃窦通道的MMC Ⅲ期缺如。
特殊测压表现模式
・餐后胃窦动力过低,与正常人相比消化不良者的收缩频率较少,收缩幅度较低,这可以导致胃排空延迟。这一表现在功能性消化不良的病人也很常见
・ 消化不良病人的MMCⅢ期常消失
・ 十二指肠运动障碍亦很常见。
胃电图
EGG可检测胃电节律的变化,消化不良的症状可能与胃电节律的紊乱有关(见8.8)。
4.4 慢性假性肠梗阻
假性肠梗阻是有肠梗阻的症状和体征,而无机械梗阻证据的一种临床综合症。
假性肠梗阻主要有两型,慢性和急性假性肠梗阻(图4.12):
・ 慢性假性肠梗阻(chronic intestinal pseudoobstruction,CIP)是一种持续几个月或数年的缩合征。疾病形成过程可能只出现于局部,也可能包括从食管到直肠的整个胃肠道。
肠梗阻症状由小肠或结肠神经肌肉功能异常引起的无效性肠推进所致
・ CIP应与急性假性肠梗阻区分。后者与急性肠梗阻相似,急性假性肠梗阻常继发于心肌梗塞、肾绞痛和急性胰腺炎等疾病。当原发病诊断明确并治愈后,急性假性肠梗阻也就很快消失。
病因
一些疾病过程可引起CIP综合征,肠平滑肌或者是肌间神经丛会受到影响。
・内脏肌病反映在肠平滑肌受累或伴有其他脏器的平滑肌异常,如虹膜、膀胱和子宫

图4.12 假性肠梗阻。
・内脏神经病变反映在肌间神经丛的异常,其比肠肌病更常见,可能伴有中枢、外周和自主神经的异常,因而,CIP可在精神迟滞、帕金森病和自主神经功能紊乱时发生。
肌病和神经病变均可分为两组:
1原发性疾病(也叫慢性特发性假性肠梗阻),是最常见的先天性起源病,包括:
・ 家族性内脏神经病变和肌病
・ 自发性内脏神经病变和肌病
2 继发性疾病
・ CIP继发于系统疾病如硬皮病、淀粉样变、肌营养不良、糖尿病、甲状腺功能减退
・ CIP继发于药物,如三环类抗抑郁药、左旋多巴、抗高血压药(可乐定、神经节阻制剂)和泻药
・ 继发于病毒感染
・ 缺血后
・ 与多发内分泌肿瘤有关
・ 伴癌CIP。
症状(图4.13)
与食管有关的症状
・ 吞咽痛
・ 烧心和GERD的其他症状。
与胃和小肠有关的症状
・ 腹痛
・ 恶心
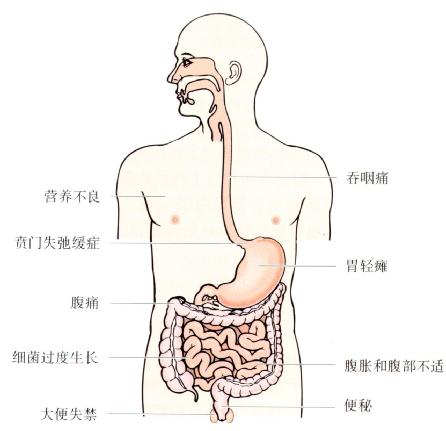
图4.13临床表现:假性梗阻可能是局限的,也可以影响整个胃肠道。
・ 呕吐
・ 胀气
・ 腹胀和腹部不适
・ 吸收和营养不良
・ 腹泻:由于细菌过度生长引起。
与结肠有关的症状
・ 排气减少
・ 便秘
・ 腹泻和便秘交叉发生
・ 大便失禁。
鉴别诊断
・ 小肠和/或结肠机械性梗阻
・ 非溃疡性消化不良
・ 肠易激综合征
・ 慢性特发性便秘
・ 妇科疾病,如:盆腔炎、卵巢肿瘤。
诊断措施
放射学
全胃肠道钡餐造影检查是除外机械梗阻非常重要的手段。在假性肠梗阻也可能显示钡剂通过延迟,提供一定程度肠道受累的一些证据。
如果胃肠道的多个部位受累,则CIP的可能性很大。
CIP肌病型的放射学表现:
・ 小肠和结肠低收缩力和扩张
・ 结肠袋消失。
在所有CIP类型中,胃部都可能增大,并有胃排空延迟(胃轻瘫)的表现(见4.2)。
转运试验
跟踪放射性试餐通过小肠可对小肠转运功能进行定性评估。而结肠转运则用不透X光的标记物进行测量。转运时间可以帮助测定肠淤积的程度和确定疾病的严重程度。
腹腔镜/剖腹探查
小肠肌病和神经病变的检查,依赖于肠壁全层样本专门的病理学活检,样本由腹腔镜或剖腹探查获得。有人认为这一方法应尽量避免,以减少与术后粘连相关性梗阻的危险。
食管测压
大部分CIP患者存在食管蠕动异常。食管异常蠕动对诊断CIP有帮助,但食管蠕动正常并不能除外CIP。并没有CIP特异的食管压力模式(见8.4)。
胃电图
EGG目前临床上不用,但研究表明EGG是区分CIP和肠神经肌病的一种非侵入性筛选试验。有报告持续性空腹胃动过速高度提示肌病性梗阻(见8.8)。
胃和小肠测压
胃和小肠测压被认为是检测CIP最敏感的诊断工具,其可在放射学、同位素和肠转运试验之前就识别出甚至是轻症患者的运动异常(图4.14)(见8.7)。
测压所见
内脏性肌病和内脏性神经病变均有运动模式异常。
・ 内脏性肌病:基础运动模式(MMC和进食反应)的整体节律正常,而单个时相压力波幅度明显减低。
・内脏性神经病变:单个压力波幅度正常,而节律异常。
神经病变性CIP异常模式包括:
・ MMC形态和传播异常
・ 时相压力活动不协调性发作
・ 不协调性压力活动持续30分钟以上
・ 食物不能诱发进食模式。
如怀疑假性肠梗阻,应按图4.15进行检查。
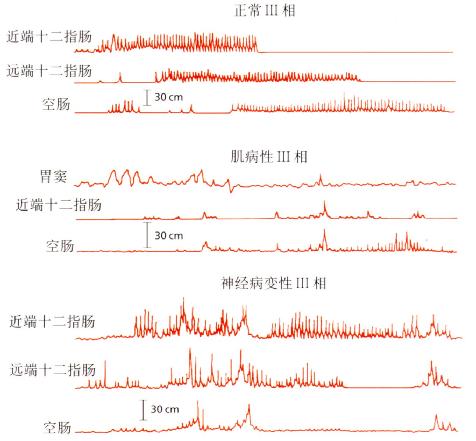
图4.14肌病性和神经病变性假性梗阻与正常人Ⅲ期活动的比较。用图经
Janssen Cilag许可,引自Motilitet i ett kliniskt perspektiv.
4.5 Oddi括约肌运动障碍(图4.16)
Oddi括约肌流出道梗阻可引起胆系症状。如果病人出现胆系症状,并记录到Oddi括约肌动力异常,就叫Oddi括约肌运动障碍。
Oddi括约肌流出道梗阻可引起胆汁和胰液在胆总管和胰管淤积,从而导致胆淤症或急性胰腺炎。胆囊排空紊乱也可引起胆结石形成。换言之,胆囊结石并不总是由梗阻引起,而是动力障碍所致的胆汁流出受阻的结果。
Oddi括约肌运动障碍常见于胆囊切除术后疼痛而无器质性病变的病人,随着胆道梗阻的证据(酶水平升高、排空延迟、胆管扩张、造影剂引流不畅)的增加,而更加增多。

图4.15 假性肠梗阻处理流程。

图4.16 Oddi括约肌的解剖。
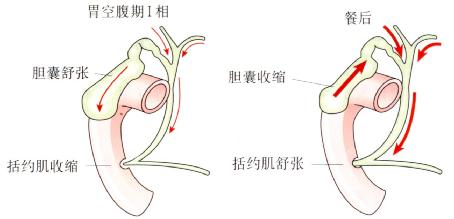
图4.17 空腹期和餐后胆管内的胆汁流向。
生理
Oddi括约肌张力和时相性收缩变化调节胆汁进入十二指肠(见4.17)。
进餐(尤其是脂餐)后需要胆汁进入十二指肠帮助脂肪吸收。胆囊肌收缩、Oddi括约肌舒张使胆汁更易流入十二指肠。
空腹期Oddi括约肌的活动更复杂。此期,Oddi括约肌存在一种基本收缩运动,使其经常处于收缩状态;此外也存在局部的十二指肠方向的收缩传递运动,以保持胆总管干燥。然而,一些正常个体,也会同时发生逆向和同步收缩,因此Oddi括约肌并非一个绝对的屏障。在空腹期,仍有少部分胆汁排入十二指肠。
Oddi括约肌运动障碍,能阻碍胆汁和/或胰液流向十二指肠,导致功能性障碍。
有关Oddi括约肌的神经激素调节知道的还很少。但已知胆囊收缩素(CCK)能抑制Oddi括约肌,从而增加胆汁流入十二指肠。
胆囊和Oddi括约肌共同的运动功能在调节胆汁酸的肠肝循环中起重要作用。也有人认为Oddi括约肌在防止十二指肠反流入胆管有一定作用。
病因
・继发于其他疾病,如系统性硬化、糖尿病、慢性特发性假性肠梗阻
・ 药物诱发的动力异常,如鸦片类等(见表4.2)
・ 特发性。
症状
上腹部疼痛和/或:
・ 右上腹痛伴有或不伴有背部放散
・ 消化不良样症状
・ 胆囊切除术后综合征
・ 复发性急性特发性胰腺炎。
鉴别诊断
・ 胆石症(胆管结石)――最常见的梗阻原因
・ 乳头炎――乳头炎症和水肿
・ 乳头狭窄――由于炎症或并发的乳头疤痕所致,从而引起Oddi括约肌舒张机制受损。
表4.2 药物对Oddi括约肌节律的影响。
| 增加括约肌节律 |
| 鸦片类 |
| 胆碱能拮抗剂 |
| α-肾上腺能拮抗剂 |
| H1受体拮抗剂 |
| 减少括约肌节律 |
| β-受体拮抗剂 |
| 抗胆碱能制剂 |
| 硝酸酯 |
| 钙离子拮抗剂 |
・ 肿瘤――壶腹肿瘤,胰腺癌
・ 慢性胰腺炎
・ 肠易激缩合征。
诊断措施
实验室分析
行实验室检查(如肝酶)以发现阻塞的任何实验室依据。
腹部超声
常作为一线检查,腹部超声检查胆囊结石可靠性很高,而对胆总管的敏感性稍低。
然而,腹部超声可以发现有胆管梗阻表现的胆管扩张。
动力超声亦可用于检测Oddi括约肌运动障碍。如果胆总管对CCK或脂餐反应在1mm或1mm以上,则提示Oddi括约肌运动障碍。
逆行胰胆管造影
逆行胰胆管造影(ERCP)是对胰腺和胆系最敏感的检查方法,ERCP可显示胆管和胰管的结构异常。ERCP时造影剂从胆总管延迟排空(>45分钟)和胆总管扩张(>12mm)提示Oddi括约肌运动障碍。
胆系同位素显像
经静脉注射放射性核素(Tc-HIDA)从肝门到十二指肠的引流延迟提示存在Oddi括约肌功能不全的可能。
测压
Oddi括约肌测压是经内镜引导将测压导管置于胆总管或胰管内,然后将导管退到括约肌的高压区(见8.14)。
测压仍是确定Oddi括约肌功能不全的金标准(图4.18)。提示Oddi括约肌运动障碍的测压表现有:
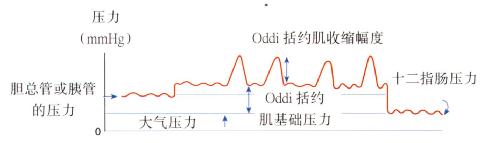
图4.18 与测压记录相关的Oddi括约肌压力示意。
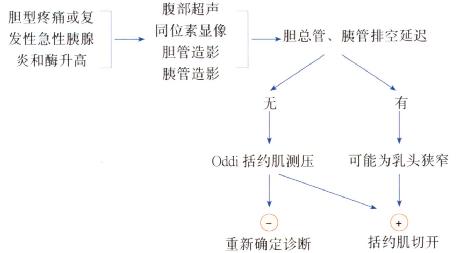
图4.19 怀疑Oddi括约肌功能不全病人诊断流程。
・ Oddi 括约肌基础压力升高――较十二指肠球腔压力高40mmHg
・ 胆管十二指肠压力梯度增加
・ 时相收缩频率增加――大于10次/分钟
・ 逆行收缩占优势(超过50%的时间)
・ 用CCK后括约肌压力不降低反而增加
・ 时相性收缩幅度增加――大于200~300mmHg。
其中,基础压力的升高是最具特异性的,而其他相关重要指标尚未确定。
图4.19是拟诊Oddi括约肌功能障碍患者的简要诊断流程图。
4.6 Oddi括约肌关闭不全
Oddi括约肌关闭不全可能导致气体或十二指肠内容物反流入胆管,引起胆管的炎症和感染。少数情况下由于细菌储留增加而出现症状(化粪池综合症)。
测压表现
・ 时相性收缩消失
・ 胆管、十二指肠压力梯度消失。
暂时性Oddi括约肌关闭不全
这种情况可能在结石由胆总管向十二指肠移行时发生。
张文俊译,许国铭校