第36章 肝性脑病
肝性脑病(hepatic encephalopathy)又称为肝昏迷或门体脑病(portal systemic encephalopathy)。它是指肝病进行性发展,肝功能严重减退,伴有(或)广泛门体短路时出现的神经系统症状和体征等。
一、病因、诱因
肝性脑病的病因分①急性肝性脑病:如暴发性、重症病毒性肝炎,药物性肝炎,化学药品如四氯化碳或毒蕈引起的中毒性肝炎,以及急性妊娠期脂肪肝。②慢性肝性脑病:见于各种病因的晚期肝硬化、门-腔吻合术后、晚期肝癌、门静脉血栓形成以及任何慢性肝病的终末期。
引起肝性脑病的诱因可归纳为三方面:①增加氨等含氮物质及其他毒物的来源,如进过量的蛋白质、消化道大出血、氮质血症、口服铵盐、尿素、蛋氨酸等。便秘也是不利的因素,使有毒物质排出减慢。②低钾碱中毒时,NH4+容易变成NH3,导致氨中毒,常由于大量利尿或放腹水引起。③加重对肝细胞的损害,使肝功能进一步减退。例如手术、麻醉、镇静剂、某些抗痨药物、感染和缺氧等。在慢性肝病时,大约半数病例可发现肝性脑病的诱因。
二、发病机制
迄今为止,肝性脑病的发病机制仍不甚明了。但动物和临床研究表明肝功能衰竭时,许多有毒物质不能在肝内代谢解毒,或由于门-体短路绕开肝脏直接进入体循环,并通过通透性增高的血脑屏障,引起脑病。这些有害物质有氨、硫醇、短链脂肪酸、过多的芳香族氨基酸、假性神经递质以及γ-氨基丁酸等,其中多数为含氮物质。
(一)氨、硫醇、短链脂肪酸 传统的氨中毒学说为众所周知。血氨增高后易进入脑内,先和α-酮戊二酸结合成谷氨酸,进而谷氨酸与氨生成谷氨酰胺。这不仅消耗ATP,且影响柠檬酸循环,减少ATP的形成,导致脑内能量代谢的障碍。但单纯的氨中毒并不直接引起昏迷,它产生中枢神经兴奋反应,表现为过度的运动和抽搐前状态,最后才导致昏迷。临床上,动脉血氨浓度和肝性脑病的程度并不都平行,血氨过高本身并不出现肝性脑病时的脑电图表现。一些研究表明,由肠道细菌产生的硫醇在血内的浓度与肝性脑病的严重程度有关。此外,短链脂肪酸的增加也加重神经症状。很可能是氨、硫醇、短链脂肪酸在肝性脑病的发病中起协同作用。
(二)氨基酸代谢异常和假性神经递质形成 暴发性肝衰竭时,血浆支链氨基酸(BCAA,包括亮氨酸、异亮氨酸和缬氨酸)浓度正常或降低,其余氨基酸浓度增加。慢性肝病时,血浆BCAA的浓度下降,而芳香族氨基酸(AAA,包括苯丙氨酸、酷氨酸、色氨酸)的浓度增高。因为肝脏为AAA代谢的主要部位,肝功能减退时,血内AAA升高。而BCAA主要在肌肉组织和脂库内代谢,肝功不全时,其代谢增快,同时血胰岛素浓度升高也促进了BCAA的降解,故血内BCAA浓度下降。AAA进入脑内后,起了真性神经递质即去甲肾上腺素、多巴胺、5-羟色胺前体的作用,因而抑制了这些生理性神经递质的合成。苯丙氨酸和酷氨酸作为酷氨酸羟化酶的底物互相竞争,过多的苯丙氨酸抑制了酷氨酸转变成多巴胺和去甲肾上腺素。脑内过量的色氨酸也增加5-羟色胺的合成,产生神经抑制作用。此外,增多的酷氨酸和苯丙氨酸在肠道内、脑内均可分别变成鱆胺和β-苯乙醇胺。它们为假性神经递质,与真性神经递质的结构十分相似,通过竞争结合于受体部位,但假性神经递质所起的作用仅为真性的1%。
研究表明,以上进入脑内的氨基酸(又称为神经性氨基酸)与脑内谷氨酰胺的增加有关。而谷氨酰胺是氨进入脑内后与谷氨酸结合的产物。因此,假性神经递质学说与氨中毒有一定的关联。
(三)抑制性氨基酸神经递质优势学说 研究表明,γ-氨基丁酸(γ-aminobutyric acid,GABA)为脑内主要的抑制性神经递质。正常时,GABA储藏于突触前神经元细胞内。只有当它释放,并与突触后神经元的GABA受体结合时,方起到抑制性神经递质的作用。肝病严重时,肠菌丛产生大量GABA,却不能在肝内得到进一步的代谢,进入脑内后,引起意识的改变。肝性脑病时神经抑制的病理生理基础是抑制性氨基酸神经递质介导的神经传导增强,兴奋性氨基酸神经递质介导的神经传导减弱。其中,抑制性氨基酸主要为GABA,还有甘氨酸等;而兴奋性氨基酸为谷氨酸、天门冬氨酸等。
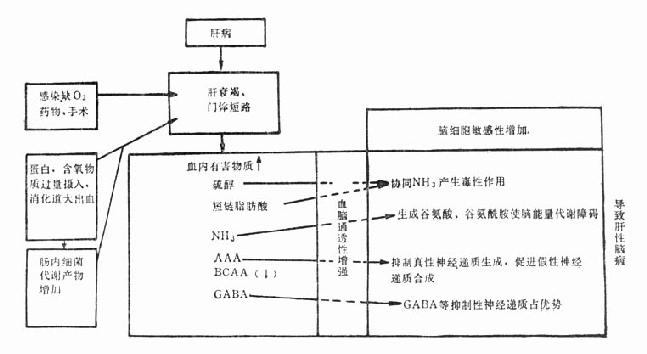
肝性脑病的发病机制错综复杂。很可能上述各有害因子的协同和综合作用导致发病(图36-1),还可能有未知因子。

图36-1 肝性脑病的发病机制
三、病理生理
肝性脑病时,不仅中枢神经系统,而且其他脏器功能也有明显改变。
(一)脑 暴发性肝衰竭时,81%~99%的患者有脑水肿。慢性肝功能衰竭时,也可发生脑水肿。这一方面是由于血脑屏障的通透性、渗透性增加,使细胞外液体增加多,出现血管性水肿。另一方面由于缺氧和毒素的作用,发生脑细胞水肿。深度昏迷患者,脑水肿加重。持续的时间越长,病变损害越难逆转。
(二)心、肺 暴发性肝衰竭、慢性肝病晚期时,心率增快,心排出量增加,周围血管阻力低,血压可低于正常。心排出量增加以保证足够的肝动脉血流。但由于肝内微循环的阻塞,使血流在肝内、外形成短路,肝血流量并不代偿性增多。肝内微循环损害、缺氧为肝功能严重减退的可能机制。同时,肝功失代偿时,肝脏不能代谢内源性或外源性的舒缩血管物质。肠血管活性肽(VIP)和P物质增加,使血管扩张,周围血管阻力下降。进而反射性刺激交感神经,使血内去甲肾上腺素和肾上腺素增多,导致不合理的血流分布。
门静脉与食管周围、纵隔、气管甚至肺静脉可形成交通短路,肺内动、静脉也形成短路,患者常有低氧血症。部分患者的肺血流异常还与高动力的周围循环有关。
(三)肾 暴发性肝炎、肝硬化晚期,尤其有大量腹水、消化道出血或合并感染时,不少患者发生肾功能衰竭,称为肝肾综合征(hepato-renal syndrome)或肝性肾病(hepatic nephropathy)。肝肾综合征与急性肾前性肾功能衰竭很相似,两者都存在肾灌注下降、尿少、尿钠排出明显下降、氮质血症。肾脏本身无明显组织解剖的异常。但肾前性者对扩容反应好,而肝肾综合征时血容量正常甚至高于正常,扩容无效。引起肾灌注不足可能与交感神经兴奋、肾素-血管紧张素系统的参与有关,更可能由于内毒素的作用,使肾血管持续收缩,肾小球滤过率下降。
(四)电解质和酸碱平衡 常见的有低钠、低钾,少尿时出现高钾。此外,还可有低镁。低钠常为稀释性的,机体总的可交换钠增加。近曲小管钠的吸收增加,同时醛固酮增加,都造成水钠潴留。此外,还可能有细胞膜缺损,使钠泵受损,细胞内钾外流,而钠内流,进一步使细胞外钠浓度下降。应用强力利尿剂时,血钠可低至110mmol/L。但一般的低钠发展慢,机体可以慢慢适应。除利尿剂引起低血钾外,其他的因素如碱中毒、醛固酮增多、胃肠道丢失钾均可引起血钾下降。肾小管酸中毒和低镁均可导致低钾血症。2%的Mg2+存在于细胞外液,从肾小球滤过的Mg2+在近曲小管回吸收。肝功能衰竭时,利尿剂阻碍Mg2+再吸收,导致Mg2+丢失。肝功能衰竭时酸碱平衡失调呼吸性碱中毒外,低钾时可伴有代谢性碱中毒。出现肾功能衰竭则有代谢性酸中毒。乳酸在肝脏内代谢,肝功能严重减退时,血乳酸浓度增高,故乳酸性酸中毒并非少见。
(五)免疫功能 急性和慢性肝功能衰竭时容易并发感染。90%网状内皮系统,包括枯否细胞,位于肝内。严重的肝脏病变使肝内网状内皮系统功能明显下降。门脉高压明显或门-腔短路术后,肝外门静脉血内细菌旁开肝脏,直接流入体循环,导致菌血症,进而细菌可入腹水,或细菌直接透过肠壁进入腹水,引起原发性腹膜炎。腹水穿刺、内镜检查、静脉输液,导尿等都容易导致各种感染,使预后凶险。
不少肝性脑病患者如晚期肝硬化,或暴发性肝炎肝实质严重损害,使肝功能衰竭,临床上不仅表现为肝性脑病,还有各脏器功能损害,这使临床表现、诊治更为复杂。
四、临床表现
(一)脑病表现 肝性脑病主要表现为意识障碍、智能损害、神经肌肉功能障碍。根据症状、体征轻重可分为四级(表36-1)。
神经系统体征表现为肌张力增强、腱反射亢进,可出现踝阵挛、扑击样震颤。有的患者作怪脸、眨眼睛,可出现吸吮等初级反射。随着病情发展,可出现锥体束征。严重时有阵发性惊厥。晚期神经反射消失,全身呈弛缓状态。
表36-1 肝性脑病的临床分级
| 级 别 | 症 状 | 体 征 | 脑 电 图 |
| Ⅰ | 轻度性格、行为异常,计算能力下降 |
(-)或(±) | (-) |
| Ⅱ | 睡眠障碍、精神错乱、行为异常、定向力下降 | (+) | (+) |
| Ⅲ | 昏睡、严重精神错乱 |
(+) | (+) |
| Ⅳ | 昏迷 | (+) | (+) |
肝性脑病如不及时治疗,尤其Ⅲ、Ⅳ级重度患者,神经损害常不可逆,症状、体征则持续存在。
脑电图上可出现异常的δ波率,两侧同时出现高电压的慢波。脑电图是一项较敏感的检查方法,但并不特异。
肝性脑病的起病、病程、表现因病因、诱因和病理基础不一而异。暴发性肝炎患者可在数日内进入昏迷,可不经过Ⅰ、Ⅱ级,预后差。肝硬化晚期消化道大出血或伴严重感染时,病情发展也很迅速。而门-腔吻合术后或门体侧支循环广泛形成时,可表现为慢性反覆发作性木僵。
(二)肝病表现 主要表现为肝功能减退、衰竭,伴有门脉高压症。前者常表现有黄疸、肝臭、出血倾向等。门脉高压症表现为门-体侧支循环形成,腹水,脾大,脾功能亢进。有些患者有门—体吻合术史。
(三)其他 包括各种基础疾病以及肝病的并发症的表现,后者如食管、胃底曲张静脉破裂出血、原发性腹膜炎、严重的电解质紊乱、肝肾综合征等。它们可以成为肝性脑病的诱因,或在肝性脑病中同时出现。
五、诊断
很难说某种临床表现或某项实验室检查能确定肝性脑病。所以,肝性脑病的诊断是基于有进行性肝病,有神经系统异常的表现,又除外了其他引起神经异常的各种病因而作出的(图36-2)。
首先要确定有无脑病存在。即患者有无意识、精神异常和神经肌肉的异常表现。脑电图为较敏感的检查,可显示异常改变。
如果有脑病,则要明确是否为肝性脑病。或者说肝病患者出现有关的神经系统症状时,要进一步明确是否有脑病和肝性脑病。肝功能减退、衰竭和门脉高压往往提示肝病为脑病的病因。有的患者脑病表现突出,但无明显的肝病病史和表现,而目前常用的肝功能试验与肝实质损害的严重性相关较差,这给诊断带来一定的困难。在各项肝功能检查中,SGOT、SGPT以及BSP试验为较敏感的试验,凝血酶原时间、血清白蛋白和胆红素常可反映肝病的严重性。有人认为测血浆凝血因子Ⅱ、Ⅶ、Ⅹ,或结合血清白蛋白为最有用的肝功能损害的指标。提示肝病而致代谢紊乱的检查有测血氨、血清BCAA/AAA比例、脑脊液谷氨酰胺、α-酮戊二酸浓度等。其他调查是为了除外其他脑病,例如BUN、血糖、电解质等。重度低钠或低镁血症可出现类似于脑病的表现,应予注意。
进而要明确肝性脑病的临床分级、急或慢性,调查了解肝性脑病的诱因和肝病的病因,估计各脏器的功能状态,以便及时处理、指导治疗和估计预后(图36-2)。
六、治疗
对肝性脑病应早期诊断、及时处理。肝性脑病的治疗是综合性、多环节的。
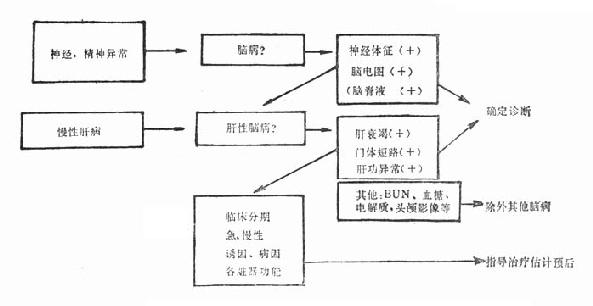
图36-2 肝性脑病的诊断程序
(一)去除诱因 许多肝性脑病有明确的诱因,这些诱因可增加血氨、其他含氮物质以及毒物的水平,促使肝性脑病的发生。因此,控制这些诱因常可有效地制止肝性脑病的发展。例如食管曲张静脉破裂大出血后可发展成肝性脑病,积极止血、纠正贫血、避免输库存血、清除肠道积血等可以制止肝性脑病的发生。合并感染时,肝功能恶化,可促发肝性脑病,而感染的临床表现可很不典型,故要警惕。对躁动的患者,主要是治疗肝性脑病,应避免使用镇静剂,尤其是苯巴比妥类药物,以免加重病情。
(二)营养支持治疗、改善肝细胞功能 肝性脑病患者往往食欲不振,或已处于昏迷状态,不能进食,仅靠一般的静脉输液远远不能满足机体的需要。
1.饮食 应以碳水化合物为主,禁蛋白质,至少3天。随着病情改善,可给蛋白质20g/d,并逐渐增加至30~50g/d,以选择牛奶、奶酪、植物蛋白为佳。每日热量不低于6278~8371kJ。可少量多次鼻饲或经中心静脉予肠道外营养。每日葡萄糖总量可达300~400g。
2.水、电解质和酸碱平衡 记录每日液体出入量,定期查血钾、钠、氯、二氧化碳结合力、血尿素氮、血细胞比积、尿钾、尿钠等。
每日入液量一般为2000ml,不宜超过2500ml。有腹水、浮肿、脑水肿者,应减少液量,并限钠,氯化钠量<3~5g/d。腹水多时,不给钠或<0.25g/d。如水潴留和低血钠同时存在,多为稀释性低钠血症,应同时限制水和钠。但如重度缺钠时,水中毒对机体造成威胁,而影响最大、危害最重的是脑神经组织,此时可给高渗盐水,同时严格限水,每日700~1000ml左右。血钠水平纠正到120mmol/L即为安全范围。此外,腹膜透析可用于纠正严重的低钠,以移去过多的水。对缺钠性低钠、低钾血症,以补钾为主,补钠为辅。进食困难者,要静脉补钾,每日给氯化钾3g,低钾碱中毒时,补钾量还要增加。如伴有低镁血症,也应予以补镁。
肝性脑病患者如出现肝肾综合征时,预后很差。要注意有无引起急性肾前性肾功能衰竭的各种因素。可试给低分子右旋糖酐、白蛋白扩容,并在此基础上,再给多巴胺以增加肾小球灌注,然后静注100~200mg速尿。应严格限制入液量,1000~1500ml/d,或以前一日尿量加上1000ml为当日输液总量。也有主张应用血透或腹膜透析,但疗效较差。
对肝功能衰竭时各类酸碱失衡,主要针对原发病因处理。
3.维生素和能量合剂 宜给予各种维生素,如维生素B、C、K,此外还有维生素A、D、叶酸。有人认为不宜给维生素B6,因为它使周围神经的多巴转变成多巴胺,影响多巴进入脑部,因而减少中枢神经系统内神经递质的形成。此外,可给ATP20mg,1~2/d,肌注或静滴;辅酶A 50u,1~2/d,肌注或静滴。
4.血浆白蛋白 胃肠道大出血或放腹水引起肝性脑病时,可静滴血浆白蛋白,25~50g/次,可维持胶渗压。补充白蛋白对肝细胞的修复也有利。
(三)减少或拮抗氨及其他有害物质,改善脑细胞功能
1.减少肠道内氨及其他有害物质的生成和吸收
(1)导泻或灌肠:清除肠道内积食或积血,减少氨、含氮物质及其他有害物质的来源,是一重要的辅助治疗。如无上消化道出血,可口服50%硫酸镁40ml导泻。肝硬化患者上消化道大出血后合并肝性脑病时,口服20%甘露醇100~200ml效果称好,能使血NH3和氨基酸浓度迅速下降。
(2)改变肠道的pH,减少NH3的形成:乳果糖和乳糖均为不能在小肠内消化吸收的双糖,在结肠内被细菌分解成乳酸、甲酸、乙酸,酸化肠内容物,使NH3变成NH+4。同时还增加肠内渗透性,起到渗透性通便的作用,加速肠内有害物质的排出。如用食醋加盐水,使pH<5,也可促进NH3变成NH+4。
(3)抗生素:可抑制肠内细菌繁殖,进而抑制毒素的形成。常用新霉素,也可口服卡那霉素、巴龙霉素或灭滴灵。不能口服时可选氨苄青霉素静滴。
(4)其他:乳酶生含乳酶杆菌,可干扰大肠杆菌生长。乙酰氧肟酸或辛酰氧肟酸抑制细菌尿素酶的作用,因而减少有毒物质产生。阳离子交换树脂可减少肠道脑毒素的形成和吸收。
2.降低血氨、减少和拮抗假性神经递质
(1)降血氨药物:如谷氨酸及其盐类能和NH3结合成谷氨酰胺,从而降低脑内NH3的氨水平。精氨酸和天门冬氨酸钾镁参与肝内鸟氨酸循环,降低血氨。可根据病情选择用药。有腹水、低血钾碱中毒时可选用精氨酸钾。还可给大剂量的维生素C,以使血略呈酸性,使血氨下降。
(2)左旋多巴:能透过血脑屏障,在脑内转化为大量的多巴胺和去甲肾上腺素,对抗假性神经递质的作用。类似的药物还有溴隐亭。
(3)BCAA:抑制并减少AAA进入脑内,减少假性神经递质产生。慢性肝病时,患者常有低蛋白血症,同时表现对蛋白质的不耐受。限制蛋白质摄取常使体内储存的蛋白质进一步消耗,而补充BCAA可减少体内蛋白分解,有可能使负氮平衡变为正氮平衡,使疾病预后改观。
3.其他 有脑水肿时,应予以脱水治疗。此外,肝性脑病患者有低氧血症,应予以吸氧,有报道,高压氧疗法可取得较好的效果。
(柯美云)
参 考 文 献
[1] 潘国宗等:肝昏迷,急诊临床,邵孝鉷、蒋朱明编:北京人民卫生出版社,1985
[2] 陈敏章等:肝硬化的水和电解质代谢。陈敏章、蒋朱明主编:临床水和电解质平衡。北京人民卫生出版社。1980
[3] 潘国宗等:水和钠的正常和异常代谢。陈敏章、蒋朱明主编:临床水和电解质平衡。北京人民卫生出版社。1980
[4] Scharschmidt BF: Acute and chronic hepatic failure with encephalopathy.In: Cecil.Textbook of Medicine.pp.845-848 17th Edition.Edited by Wyngaarden JB and Smith LH ,W B Saunders.1985
[5] Jones EA: Potential neural mechanisms in the mediation of hepatic encephalopathy.In: Edited by Roger Williams;Live Failure.Longman Group Limited,Churchill Livingstone,1986
[6] Ede RJ et al: Occurrence and management of cerebral oedema in liver failure .In: Edited by Roger Williams;Liver Failure.Longman Group Limited,Churchill Livingstone,1986
[7] Bihari DJ et al: Disturbances in cardiovascular and pulmonary function in fulminant hepatic failure.In:Edited by Roger Williams;Liver Failure.Churchill Livingstone,1986
[8] Ring-Larsen H: Associated renal failure.In: Edited by Roger Williams;Liver Failure.Churchill Livingstone.1986
[9] Rimola A et al:Infective complications in acute and chronic liver failure:basis and control.In: Edited by Roger Williams;Liver Failure. Churchill Livingstone,1986
[10] Morgan MY:Amino acids in hepatic failure.In: Edited by Roger Williams;Liver Failure Churchill Livingstone.1986