�ڶ��ڡ�ƶѪ
��Anemia��
�����š���
������һ���ݻ���ѭ��ѪҺ�ں�ϸ��������Ѫ�쵰�����Լ���ϸ��ѹ���������������߳�ΪƶѪ��������Ѫ�쵰����Ϊ��Ҫ���������Ե���120g/L��12.0g/dl��������Ů�Ե���110g/L(11.0/dl)��һ�����ΪƶѪ��
����ƶѪ���ٴ�����ı���֮һ��Ȼ��������һ�ֶ���������������һ�ֻ����Ļ���ʱ�ǽϸ��Ӽ�������Ҫ�ٴ����֣�һ������ƶѪ����������䷢��ԭ��
�������ݹ��ڵ������ϱ�����������ѪҺ�ں�ϸ����Ѫ�쵰����ϸ��ѹ����������Χ���£�
��5��2��1 ��ϸ����Ѫ�쵰����ϸ��ѹ��������Χ
| �� | ��ϸ������1012��L�� | Ѫ�쵰�ף�g/L�� | ��ϸ��ѹ�� |
| �� | 4.0-5.5 (400 550��mm3) |
120-160 (12-16g/dl) |
0.4-0.5 (40-50�ݻ���) |
| ٠| 3.5-5.0 (350-500��mm3) |
110-150 (11-15g/dl) |
0.37-0.45 (37-45�ݻ�)�� |
��������������Χ�����ŵ����������������ԭ�ľ�������ֵ�ϸߡ�����ʧѪ�����ڣ���ϸ����Ѫ��ͬʱ�ɱ������٣����Ѫ�쵰��ֵ�����������Ѫֹͣ��Сʱ��Ѫ���������ӣ�ѪҺ��ϡ�ͣ�Ѫ�쵰�ײ��½����������ߺ�ϸ�����ࡣ��Ѫ����ʱ����Ѫ�������ӣ���Ҫ������Ѫ���������ӣ�Ѫ�쵰��Ũ����Լ��ͣ���ϸ���ľ�������δ�ı䡣������ٴ�������ȷ������ƶѪ���������������⣬��Ӧ��ϻ��ߵľ�������ۺϿ��ǡ�
��������Ѫ�쵰���ͳ̶ȵIJ�ͬ���ٴ��Ͻ�ƶѪ��Ϊ����4����
��5��2��2 ƶѪ���ٴ��ּ�
| �ּ� | Ѫ�쵰�ף�g/L�� | �ٴ����� |
| ��� | 120��91(12��9.1g/dl) | ֢״�� |
| �ж� | 90��61(9��6.1g/dl) | �����Ͷ���е��Ļš����� |
| �ض� | 60��31(6��3.1g/dl) | �Դ���ϢʱҲ���Ļš����� |
| ���� | <30(3.0����g/dl) | ���ϲ�ƶѪ�����ಡ |
����ƶѪ�IJ�������
������ϸ������Ҫ��������������������ѪҺһ��Ѫ�쵰����Я��1.34ml����ƶѪ�IJ�������������ѪҺЯ���������ͣ���֯ȱ���������ȱ�����д�������Ӧ�������£�
����һ�����ಫ�������ӡ�
����ƶѪ�������ϸ�����٣�ѪҺճ�ȼ��ͺͺ�ѡ���Ե���ΧѪ�����ţ���ΧѪ���������ͣ����ʼ��٣�ѭ���ٶȼӿ죬Ϊ��ֹ�Ի��幩�������٣�������Ѫ�����ӡ�
��������������֯�Ĺ�ע��
����ƶѪʱѪҺ��Ӧ���·��䣬��Ѫ��������ΪƤ����֯�����࣬��Ƥ���ף���ȱ�����е��ļ����Ժͼ��Ѫ�����ӡ�
���������εĴ������ܡ�
����ƶѪʱ�����ӿ졢���������ǿ�����Ⲣ���ܵõ����������������Ƕ���֯ȱ����һ�ַ�Ӧ��
�����ġ���ϸ�����ɿ���
����ƶѪ���߳������ϰ���ƶѪ�⣬�������к�ϸ�����ɿ������Һ�ϸ�������صIJ���Ҳ���ӣ�һ���ϸ�������ص��ͷ����ϸ��������Ѫ�쵰��Ũ�ȳɷ��ȡ�
�����塢�������������ơ�
�����ڻ���������ƶѪ����ϸ����2��3����������ᣨ2��3��DPG���ĺϳ����ӣ�2��3��DPG��������Ѫ�쵰��ϵ�������ʹѪ�쵰���������������ͣ��ٽ�HbO2�����������ƣ�ʹ��֯������ѹ���͵����������ȡ���������
��������BohrЧӦ��
����ƶѪʱȱ���������������֯�����ǽͽ⣬����������ѻ�������֯���ж���Ѫ�쵰���������������ͣ������ͷ����࣬���ʹ��֯�������ơ�
����ƶѪ����
����ƶѪ���Ը��ݺ�ϸ������̬�ص������ԭ��ͷ����������Է��ࡣ
�������ݺ�ϸ����̬�ص���࣬��Ҫ�Ǹ��ݻ��ߵĺ�ϸ��ƽ�������MCV������ϸ��Ѫ�쵰��ƽ��Ũ�ȣ�MCHC����ƶѪ�ɷ�Ϊ���ࣺ
����һ����ϸ����ƶѪ��
������ϸ��MCV��95fI������ƶѪ���Ϊ����ɫ���ͣ���Ҷ���ά����B12ȱ������ľ���ϸ����ƶѪ��ƶѪ����֯��ϸ����������ʱ��
����������ϸ����ɫ����ƶѪ
������ϸ��MCV��80��95fI��MCHC��0.32��0.36(32��36%)��������ƶѪ���������ϰ���ƶѪ��������Ѫ��ƶѪ������ʧѪ��ƶѪ������ϵͳ�Լ�����������֢����Ⱦ����֢���β��������֯���������������ڷ��ڲ��ȣ��鷢��ƶѪ�ȡ�
��������Сϸ����ɫ����ƶѪ
������ϸ��MCV��80fI��MCHC��0.31(31%)�����ڴ���ƶѪ����ȱ����ƶѪ��������ƶѪ��������ϸ����ƶѪ�ȡ�
����������̬���෨���������ϸ��ָ���⣬��Ӧǿ��ѪƬ�Ĺ۲죬��Ϊ��ϸ����̬�ĸı���ѪƬ����Ϊ��������ϸ����ƶѪ������ζ�����к�ϸ������������С�����Һ�ϸ����С���ȿ��ܺ����ԣ�����ƽ�������������Χ�ڡ���ϸ����ƶѪ��Ҳ���в���Сϸ�����֡����⣬��̬�ı������ϸ��Ҳֻ����ѪƬ���ܹ۲쵽��
�������ݲ���ͷ��������ķ��࣬ƶѪ�ɷ������5��2��3��
������������ƶѪ���෨���о����ԡ���̬���෨��ȱ����ƶѪ��Ҷ��ȱ����ά����B12ȱ���ľ���ϸ����ƶѪ��������ṩ��Ҫ������������ϸ����ƶѪ���ȷ����ϵ�������������෨���ŵ��Ƕ�ƶѪ�����Ļ�������˵��������ijЩƶѪ�ķ��������Ƚϸ��ӣ�������һ��ԭ���������ƶѪ��ȫ��������
��5��2��3 ƶѪ�IJ������
| һ����Ҫ���ں�ϸ�����ɼ������µ�ƶѪ |
| ��һ����Ѫ��ϸ����ֳ�ͷֻ��ϰ� 1�������ϰ���ƶѪ��2�����������쳣��ƶѪ |
��������ϵ��ϸ����ǰ��ϸ����ֳ�ֻ��ϰ�
3���ڷ��ڼ����鷢��ƶѪ�� 4�������Ժ�ϸ�������쳣��ƶѪ |
| ������DNA�ϳ��ϰ�������ϸ����ƶѪ�� |
| ���ģ�Ѫ�쵰�ϳ��ϰ�����ɫ����ƶѪ�� |
| ���壩���ֻ��ƻ�ԭ��δ�� |
| ������Ҫ���ں�ϸ���ƻ������ʧ���µ�ƶѪ |
| ��һ����ϸ���ڲ��쳣 1��Ĥȱ�� ��1���Ŵ������κ�ϸ������֢����2���Ŵ�����Բ�κ�ϸ������֢ ��3���Ŵ��Լ��κ�ϸ������֢�Ϳ��κ�ϸ������֢ |
| 2��øȱ�� ��1�������ǣ�6-��������øȱ�� ��2����ͪ�ἤøȱ��������øȱ�� ��3��߲��֢ |
| 3���鵰���쳣��Ѫ�쵰�ײ��� ��1����״ϸ�������йؼ��� ��2�����ȶ�Ѫ�쵰�� ��3����������Ѫ�쵰�ײ� |
| 4������˯����Ѫ�쵰���� |
| ��������ϸ���ⲿ�쳣 |
| 1����е�� ��1���о���Ѫ�쵰������˶���ƶѪ ��2�����ഴ������Ѫ��ƶѪ ��3��Ѫ�ܲ�����Ѫ��ƶѪ |
| 2����ѧ�������� ��1�����ڻ�ѧ�����������������Ѫ��ƶѪ |
| 3����Ⱦ ��1�����������Ⱦ�������Ѫ��ƶѪ |
| 4������鵼�� ��1�������·�Ӧ�����������»������Ѫ��ƶѪ ��2�����������ۺ��� ��3����������Ѫ�쵰���� ��4��ҩ���շ�����������Ѫ��ƶѪ ��5��������ͬ��[����] ��������Ѫ�Լ��� |
| 5�����˾���ϸ�����ܿ��� Ƣ���ܿ��� |
| 6��ʧѪ ����ʧѪ��ƶѪ |
�����ٴ�����
����ƶѪ֢״���������أ�ȡ����ƶѪ�ij̶ȡ�ƶѪ�������ٶȡ�ѭ��Ѫ�����ı䡢���˵������Լ���Ѫ��ϵͳ�Ĵ��������ȡ�ƶѪ��������������������Ӧ����ʹƶѪ���أ��п�ά���������ܣ���֮��������ڷ���ƶѪ����ʹƶѪ�̶Ȳ��أ�Ҳ�ɳ�������֢״�������������ġ��ι��ܼ����ߣ�֢״�����ԡ�
����ƶѪ��һ��֢״���������£�
����һ����������
����ƣ�������룬������ȱ�����¡�Ϊ�����������ֵ�֢״��
��������Ƥ����ճĤ��
����Ƥ����ճĤ����Ĥ�Լ�Ƥ��ëϸѪ�ܵķֲ�������״̬�����ص�Ӱ�졣һ����Ϊ�����Ĥ�����ƴ�С��ʼ��״�����ɫ�ȽϿɿ���
����������Ѫ��ϵͳ��
�����ļ�Ϊ��ͻ����֢״֮һ�����Ķ����٣����ļ��ζ���������������͵���������������ΪƶѪ��������hemic murmur��������ƶѪ����������������������ƶѪ��ԭ�й��IJ����������Ľ�ʹ��������������˥�ߡ�
�����ġ�����ϵͳ��
����������������ѣ��������ں�������������̼��Ѫ֢���¡�
�����塢������ϵͳ
����ͷ�Ρ�ͷʹ���������ۻ���ע���������С���˯�Ⱦ�Ϊ����֢״������������־ģ���ɳ�����ƶѪ���ػ��������ߣ��ر������껼�ߡ�
������������ϵͳ��
����ʳ�����ˡ��������������ġ����ص�Ϊ������֢״��
�����ߡ���ֳϵͳ��
������Ů�����г����¾�ʧ������վ����¾����ࡣ����Ů�������������˾������
�����ˡ�����ϵͳ
����ƶѪ�����߿�����ȵ�������Ũ�����ܼ��͡�
�����š�����
����ƶѪ����ʱ�������ѭ����������Ƥ��ɢ���������ˣ����е��ȡ�
�������
����ƶѪ����������Ѫ�쵰�ײⶨ����ȷ�������ƶѪ��ԭ��ʮ����ҪҲ�����ף��мɽ�ƶѪ�����������Ϊһ�����ļ���������Ϲ�����ע�����¼����棺
����һ����ʷ��
������ϸѯ������ƣ��������������ͷʹ��ѣ�Ρ����ʡ��ļ¡��������ѣ�����Ѫʷ��ŻѪ���ڱ㡢���ɫ���ڸ�Ů�������¾����࣬������������������Ͳ������������Ӫ��ȱ����ƫʳ��������ֺ�������������뻯ѧ�����������ʽӴ�����ǰ������������ƶѪ��ҩ�������ʾ��������֢����Ⱦ���������β���������������ԭ�Լ������ڷ��ڹ������ҵȼ�����֢״�������������к�ƶѪ�����������κ�ϸ������֢���Ŵ��Լ������ߡ�
������������顡
������ȫ�����⣬��ע������Ƥ���ף���Ĥ�ף����㣬�ܰͽᡢ�Ρ�Ƣ�״���ѹʹ��������쳣�ȡ��������׳��������ص�ȱ����ƶѪ������ͷή���ͼ����������������������ά����B12ȱ�����������Σ���������Ѫ��ƶѪ��
��������ʵ���Ҽ��
��������ϸ����Ѫ�쵰�ס���ϸ���Ȼ��⣬�������ѪҺѧ���Ӧ������
������һ��������ϸ��������У����֯��ϸ�����������ߵĺ�ϸ��ѹ����0.45/L����֯��ϸ����������
����������MCV��MCHC �IJⶨ��
��������������ѪͿƬ���۲��ϸ���������κ�ϸ���������κ�ϸ�������κ�ϸ������ֳϸ��������ϸ����С��������ɫ�غͶ�Ⱦ�Ժ�ϸ�����ȼ��Ե�ʡ�����������һ����С��ȡ���ϸ����ѪС����������̬ѧ����ĸı䣬�����쳣ϸ����
�������ģ����贩��������ͿƬ��飬����ϲ���ȱ������ҪʱӦ�������졣������������Ⱦɫ����ȷ����ų�ȱ����ƶѪ��������ϸ����ƶѪ������̬ѧ����Ļ����ϣ���Ŀ�ĵ�ѡ��ijЩ�����飬���������Ѫ�Լ��������飬��ȷ����ϡ�
�����ġ��������
�����桢�����Ѫ���������ѡ�ѪҺ���ص���Ѫ�����Լ��β�X���Ⱦ����ݺ��ӡ�
��������
����һ����������
��������ƶѪ��ԭ�����ز�ȡ�ʵ���ʩ���������ܶ�ʱ��ԭ������ƶѪ������Σ�����صöࣨ����θ�������ף���������Ҳ��ƶѪ��Ϊ��Ҫ���ڲ������δ��ȷʱ����Ӧ��Ͷҩ��ʹ������ӣ���������ϵ����ѡ�
��������ҩ�����ơ�
�����м����ò�Ѫҩ�������ϸ����ո���ҩ�����Ӧ֢������ά����B12��Ҷ�����������ƾ���ϸ����ƶѪ������������ȱ����ƶѪ���������ڷ�ȱ����ƶѪ��������������ɹ��أ�Ӱ����Ҫ���٣����ġ��Ρ��ȵȣ��Ĺ��ܣ�ά����B6����������ϸ����ƶѪ��Ƥ����̴�������������������Ѫ��ƶѪ��غ��ͪ���������ϰ���ƶѪ�ȡ�
����������Ѫ��
������Ѫ��Ҫ���ŵ�����Ѹ�ټ�������ƶѪ�����Դ���ʧѪʱ����Ѫ�Իָ�����Ѫ���ͳɷּ�Ϊ��Ҫ���κ�����ƶѪ��ҩ���������ʩԤ�Ʋ�����������ЧӦ��һʱ����Ч�ߣ�Ϊ��Ѹ�ټ���ȱ��֢״�ೣ��Ҫ��Ѫ������Ѫ���Ǿ�����ȫ������Ѫ���������ƹ�����Ѫ���ܵ����á���Ѫ��ʱ�������������������ķ�Ӧ�������Ѫ���Ӵ�Ⱦ�����Ը��Ļ���ͻ�������ɹ��ص�Σ�ա���˱�����ȷ������Ѫ����Ӧ֢�����������Ѫ��Ϊ�˼�����Ѫ��ϵͳ�ĸ��ɹ��ͼ�����Ѫ��Ӧ������עŨ����ϸ����
�����ġ�Ƣ�г���
����Ƣ�����ƻ�Ѫϸ������Ҫ���٣��뿹��IJ���Ҳ�йء���������ƶѪ��Ƣ�г���ϸ��������ʱ���ӳ���ƶѪ��Ѹ�ٵõ���������Ч���ܹ��̣������Ŵ�������ϸ������֢��Ƣ���ܿ��������ƶѪ������ЩƶѪƢ�г�����Լ��ᣬ��Ҳ���Բ����ԣ�������Ӧ���㹻֤�ݱ�ʾƢ���ƻ�����ĺ�ϸ��������Ӧ���ʵؽ���������
�����塢������ֲ��
����������ֲ�ǽ�����һ���µ�ҽ�Ƽ�����Ŀǰ�����о����ýΣ���Ҫ���ڼ��������ϰ���ƶѪ֮����δ����Ѫ�������Ѫ�IJ��ˣ������ֲ�ɹ������ܻ��������
ȱ����ƶѪ��Iron Drficiency Anemia��
����ȱ����ƶѪ��ָ���ڿ���������Ѫ�쵰���������ѱ��þ�����ϸ�������ϰ����µ�ƶѪ���ص��ǹ��衢�Ρ�Ƣ��������֯��ȱ����Ⱦɫ����Ѫ��������Ũ�Ƚ��ͣ�Ѫ����Ũ�Ⱥ�Ѫ��ת�����ױ��Ͷ�������͡�����ΪСϸ����ɫ����ƶѪ��
�����������
����ȱ����ƶѪ��������һ��ƶѪ���㷺�ش�����������أ�������������֯��WHO�����鱨�棬ȫ����Լ��10�D30������Ⱥ�в�ͬ�̶ȵ�ȱ�������Է�����Լ10����Ů�Դ���20�����������ʸ���ŷ�ޡ�����������ĸ�Ů���ر����и�����Ӥ���У�����ƶѪ�ķ������ܸߡ��ڹ��没���е�����ɣ���ء�����ֲ������ȱ����ƶѪ���������ƶѪ�ij̶�Ҳ���أ�����������ҽҩ���������ĸ��ƣ�ũ�徭������ĺ�ת��ȱ����ƶѪ���ҹ��ķ�����������س̶Ƚ������Ժ�ת��
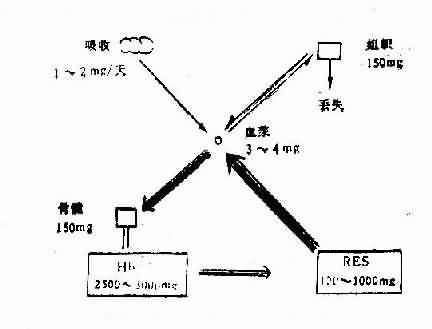
�������Ĵ�л
������������Ѫ�쵰��ԭ�ϣ������������ں�����Ϊ3��5�ˣ������䡢�Ա����صȶ����в��졣����65��ΪѪ�쵰������30������������Ѫ���ص���ʽ�����ڸΡ�Ƣ������ȵ��˾���ϸ��ϵͳ�У���ʱ��ӦѪ�쵰�ĺϳɣ�����5��Ϊ��֯���������ڼ��쵰�ס�ϸ��ɫ�غ�ϸ���ڶ���ø�С���Ѫ������ת������ϵ�����ռ0.12�����ң������������Щ��ͬ��ʽ��������������ȶ�����ֵ��
����������������������Դ����ʳ�����ʳ���֬�������ࣩ�ж��������������������Ϸḻ��ʳ���к��������ˡ��ϲˡ�ľ�����㹽������Ρ����ࡢѪ������ȡ�����ʹ����ˮ�����߲��к������ϵͣ��麬�������͡�
��������ʳ���е���Լ10��25���ܱ����գ���ֲ���е����ܱ������߽�Լ1��������ʳ���м��쵰��Ѫ�쵰���е�Ѫ���ؿ��������ķ���ֱ�ӱ��������գ��������������ʽ�ĵĺ������ʣ�����ֲ���е�������������θ��ʮ��ָ����ת�������Ķ��������ܱ����ա�����������������ղ��DZ�Ҫ�������Ե�θҺ�ܷ�ֹ�����ӱ�ɲ�����ˮ���������ά����C�����ԭ����ʹ������ԭ������������������ȸ����ױ����ա�ʮ��ָ����С���ϲ���������������ߡ��������볦ճĤϸ���ڵ�ȥ������϶������ա�С�������������ٶ��е�������������������������ʧʱ����ϸ�����ɼ���ʱ�Լ�ijЩ����״̬��Ѫɫ������Ӳ���ȣ��������������ࣻ��֮�������������������ʱ��Ѫɫ�����⣩����ϸ�����ɼ���ʱ�����и�Ⱦ��ȫ��Ӫ��״̬�����Լ�θ��ȱ�������ʱ���������ռ��١�������ǻ������Ũ�Ⱥܸߣ���ڷ�����ʱ��С����ʧȥ���ĵ��������������������ͨ����ɢ���볦ճĤϸ������ˣ��������������ο������������ж���

ͼ5��2��1 ��������л����Ҫ;��
�����ڳ�ճĤϸ���ڵ�����Ѫ��ת�����ף�һ�֦�1�ף���Ϻ���Ѫ���б�����������֯����Ҫ�ǹ����ڵ���ϸ��������Ѫ�������ϵĦ�1������Ϊ�ܽ���������������ת������Լ1/3������ϣ���1��3���ͣ�����ΪѪ������Ѫ����������2/3������������δ������ϵ���DZ�ڵĽ�����ߣ���Ϊδ���͵��������������Ѫ�������Ͷ���ָ�����������Ѫ������ռ�ٷֱȣ�����5��2��4����
��5��2��4 �������ⶨ������ֵ
| ��Ŀ | ���� | Ů�� |
| Ѫ������umol/L�� | 9��29(50��160ug/dl) | 7��27(40��150ug/dl) |
| �����������umol/L�� | 45��72(250��400ug/dl) | |
| Ѫ�������Ͷ� | 0.20��0.55(20��55%) | |
����ע δ������������������������Ѫ����
����Ѫ�������Ͷȣ�Ѫ��ת�����ױ��Ͷȣ�=(Ѫ��������)��(���������)��100(%)
��������������£��������պ���й����ƽ��״̬������ɥʧ��������������������ÿ��һ�㲻����1mg�������¾���Ů�У�ƽ��ÿ��Լ2mg��ƽʱɥʧ����й��;����Ҫ��ͨ����ճĤ��Ƥ�������ϸ����������Ҫͨ���¾�������Ͳ����ɥʧ�϶�������ݹ���һ�������¾�ʱ��ɥʧ����ƽ��ԼΪ17mg ��һ����������ʧ��Լ700mg��ƽ��ÿ��ɥʧ��2.5mg ��������ÿ�վ���֭��ʧ��0.5��1mg���ڲ�������£�ʧѪ��ɥʧ������Ҫԭ������Ѫ������Ѫʱ��������Ҳ���Ժ���Ѫ���ػ�����Ѫ�쵰����ʽ�����ų����⣨��ͼ5��2��1����
��������������
����ȱ����ƶѪ�ɷ��������м��������
����һ��������Ҫ�����Ӷ����벻�㡡
�������������ٵ�Ӥ������ͯ���¾����ࡢ�����ڻ����ڵĸ�Ů��������Ҫ�����࣬�����ʳ��ȱ������������ƶѪ���������顢��������飬���ĺ������ܵͣ�0.1mg%��������ʳ�����ס��桢�����Ⱥ�����Ҳ�ܵ͡����������ἰ�������������������γɸ����ʹ�����ױ����ա��ʰ˸������ϵ�Ӥ�����������������ʳ��Ϊ��ҪӪ����������ȱ����ƶѪ���ഺ�ڵ�Ů�������¾��������׳���DZ��ȱ�����¾����࣬�������Ͳ����ʹ������Ů����ȱ����ƶѪ��
���������������ղ���
���������������ϰ�������ȱ����ƶѪ�߱Ƚ��ټ�����θ��ȫ�г���������ʳ��Ѹ�ٽ���ճ�����ʳ���е���û�о�ʮ��ָ�������գ��ɷ���ȱ����ƶѪ�����ֲ�ͬԭ������ij������ظ�к������θ��ȱ��Ҳ��������ȱ����ƶѪ��
��������ʧѪ��
����ʧѪ������������ʧѪ����ȱ����ƶѪ����������Ҫ��ԭ����������Ѫ�������������没��ʳ���������ų�Ѫ���̳�Ѫ������ˮ�����κ���θ����Լ��������������Գ�Ѫ�ļ�������Ů�¾��������Ѫ��ƶѪ�麬��Ѫ�������Ѫ�쵰����Ⱦ�������ȱ����ƶѪ��
����ȱ����ƶѪ�ķ�����һ���ϳ�ʱ�������γɵġ����Ľ��ڣ��������ľ���Ѫ���������ͣ���ʱ����ƶѪ����ȱ����һ�����ء��������ľ���Ѫ��������Ѫ�����½���������������ߣ�ת�����ױ��Ͷ��½���������ϸ��ȱ���������ϸ��ԭ߲�����ӣ�Ҳ�������Բ�ƶѪ��Ǧ�ж�����ϸ������ԭ߲��֢��������ϸ����ƶѪ�ͺ�ϸ�������������ӵ�״̬����״ϸ����ƶѪ�������С��ϸ������Ϊȱ����ϸ�������ڣ�ȱ���ٽ�һ����չ�������ϸ��ԭ߲�����ߣ���Сϸ����ɫ����ƶѪ����Ϊ����ȱ����ƶѪ����ͼ5��2��2����
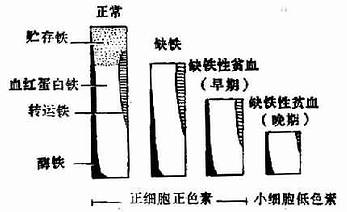
ͼ 5��2�D2 ȱ���ķ�չ��
��������ȱ����������ѪҺѧ���쳣��������Σ�Ѫ����Ũ��ż������������������������ȱ������ȱ����һ����չ��ƶѪ�Ⱥ�ϸ����̬�ı��ȳ��֣�������һЩϸ���ɱ�����ϸ��С��������ϸ���ס�Ѫ����Ũ�ȳ����ͣ���Ҳ������������ȱ���γʵ��͵�Сϸ������ɫ�ء�Ѫ�������͵�ƶѪ��
����ȱ��ʱ�����Ⱥ���Ѫ���غ��������ڹ�����������洦��ʧ������������Ҫ���������Լ��ͣ���ϸ��ɫ��C��ϸ��ɫ������ø������������ø����ͷ��ø������������ø�����쵰�ȣ������ȱ��ʱ��������֯ϸ����л�ͻ��ܷ������ҡ�θճĤ�������᳣���١�43��ȱ�����߿ո���֯��������ʾθ��ȱ�����в�֪θ��ȱ���������ղ�����ԭ����ȱ����ή����θ��θ��ȱ����ԭ����ϵͳ�����ϰ���ȱ���Ļ��ߵ�������ø���Լ��ͣ��ɵ���������������
������֯ѧ���֣���������Ѹ����ֳ��ϸ����ȱ���ر����У��ࡢʳ�ܡ�θ��С��ճĤή������ճĤ�䱡����Ƥ�ǻ����ʺ�ճĤή�������ڻ�״���Ǻ������γ��룬��˲���ȱ�����������ѣ�Sideropenie dysphagia������Plummer-vinson�ۺ�������Paterson-kelly�ۺ�������
�����ٴ�����
���������ٴ������Т�ԭ�������ٴ����֣���ƶѪ���������֢״�������ں���ø����������ʹ��֯�������ں����ϰ��������֢״����ǰ���߲�������
����һ����Ƥ��֯�������֢״��
����ϸ���ں���ø���٣�����Ƥ�仯����Ҫԭ��
������һ���ڽ��������ס�Լ10��70�������пڽ��ס�����⻬������ͷή�����������������ԡ�
����������ʳ���롡��״���Ǻ��ʳ���룬������ʳ����Ƥ����ϸ�����������Ա�ͽǻ�������������ʱ����Ӳ���У�Plummer-vinson�ۺ����������ҹ��Ƚ��ټ���
����������ή����θ����θ��ȱ��
�������ģ�Ƥ����ָ�ױ仯��Ƥ������ǻ���ή����ë�����������䣻ָ�ײ���������ƽ�ף����ͻҼס�
����������ϵͳ����֢״��
����Լ15��30�����߱�����ʹ����ͷʹΪ�������о��쳣�������߿�����ѹ���ߺ�����ͷˮ�ס�5��50�������о�����Ϊ������쳣������ע���������У�������������ͺ���ʳԭ����ȱ������Ӱ������֯��������л��������Ҳ�ܵ�������Ϊ�йص������嵥��������ø�Ļ��Խ��͡�
��������Ƣ�״�
������ԭ�����ϸ�����������йء�
����ʵ���Ҽ��
����һ��Ѫ��
�������ڻ����ȱ������û��ƶѪ��������ƶѪ�����ڻ�����ȱ���е��͵�Сϸ����ɫ����ƶѪ����ϸ��ѹ����Ѫ�쵰��Ũ�Ƚ��͵ij̶�ͨ����ϸ���������ٵij̶ȡ����ɼ����ٵİ��Ρ���Բ�λ�������������̬�ĺ�ϸ������֯��ϸ�����������������ϸ��������������ȼ��͡�ѪС������ߵͲ�һ��
��������������
��������������Ծ������������ͣ���ϸ��ϵͳ�������Ի�Ծ������ϸ���������࣬�����һ�������ϸ����С����Ե�����룬�����٣�Ⱦɫƫ�����˹���������ϸ��������������������ںˣ���ϵϸ���;�ϸ����������̬��������
��������������Ⱦɫ��
��������³����Ⱦɫ�ɼ����躬��Ѫ�������ԣ�����Ϊ+��++����������ϸ�����Ի���٣�����Ϊ20��90%����
�����ġ�Ѫ�������ס�
���������������ڴ�������һ����ʽ��Ѫ��������Ҳ���������������ã�ͨ��1ug/L���������д�����8mg����Ѫ�������IJⶨ�ǹ��ƹ���������״̬��һ�����еķ�����Ѫ������������ֵΪ100��60ng/ml����ȱ����ƶѪʱС��15ug/L��15ng/ml����
�����塢Ѫ������
����ȱ����ƶѪʱѪ����������10.74umol/L(60ug/100ml)��������������ߣ�����64.44umol/L(360ug/100ml)��Ѫ�������Ͷȼ��٣�����15����ͼ5�D2��3����
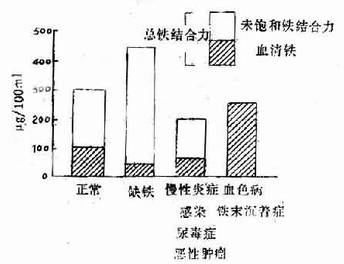
ͼ5��2��3 ���������Ѫ�������������
����������ϸ������ԭ߲����FEP����
��������Ϊ0.29��0.65umol/L(16��36ug/dl)��ȱ��ƶѪʱ���ߡ����⣬����Ѫ���غϳ��ϰ��ļ�������Ǧ�ж���������ϸ����ƶѪʱ��FEP�����ӣ���FEP����Ϊ��ɸ���顣
������ϼ��������
�������ݲ�ʷ��֢״��Сϸ����ɫ����ƶѪ�������ϵͳ������ϸ��������ʧ��ϸ���������ٻ���ʧ��Ѫ���������١�Ѫ�������͡�������������ߡ������Ͷ��½��ȡ�ȱ����ƶѪ��ϲ��ѡ���ȷ���������ȱ��ԭ���������м�������
����һ�����Ը�Ⱦ���µ�ƶѪ��
����һ��Ϊ��ϸ����ɫ��ƶѪ�������Ϊ��ȵ�ɫ�ԡ�Ѫ����Ҳ�ǵ͵ģ���Ѫ����������������߷������ͣ������������ò�����������ϸ��������Լ��٣�������ȫ��ʧ�������������������࣬���躬��Ѫ���ؿ����������࣬һ��ɲ����ȷ�ĸ�Ⱦ�����������������Ⱦ�������ס���ǻ�ס���˲��������Ⱦ�ȡ�
��������������ƶѪ��
���������ڹ���Ѫ�쵰���鵰�������ϳɼ������£��м���ʷ��Ϊ��ͬ�̶ȵ�Сϸ����ɫ����ƶѪ��ѪƬ�м��϶����ϸ����Ѫ���������躬��Ѫ���غ�������ϸ�����������࣬Ѫ�쵰��Ӿ�쳣��
��������������ϸ����ƶѪ��
������������ϸ����������ø��ȱ���������ò��������ܺϳ�Ѫ���أ������Ѫ�쵰�ϳ��ϰ�������Ҳ�е�ɫ����ƶѪ����Ѫ�������ӣ�������������ͣ������ں���Ѫ���غ�������ϸ�����������࣬����������Ļ���������ϸ������������塣
��������
��������ȱ����ƶѪ��ԭ���ǣ��ٲ������ƾ����ܳ�ȥ����ȱ����ƶѪ��ԭ�ڲ����㹻�������Թ�����ϳ�Ѫ�쵰�ף�������������������������ˮƽ��
����һ���������ơ�
�����������ƶԾ���ƶѪ��Ч�����ٶȼ���ֹ�临��������Ҫ���壬��˱������ӣ�����ƶѪ�����ƿ�����ȫ��Ч����Ч�����ԣ���һ��������ܺ������ص�ԭ�������������ڰ��ȣ�����������ʱ����
���������������ơ�
�����пڷ���ע����������
������һ���ڷ���������õ��Ƽ�Ϊ�������������˼���Ϊÿ�����Σ�ÿ��0.2��0.3g(ÿ0.1gFeSO4��7H2O����20mg)��������������Ѫ�ᣩ0.2/Ƭ��Ԫ����66���ˣ�ÿ��1��2Ƭ��ÿ�����Σ�����ʱ���,���Լ���θ�����̼��������в��ʣ����Ƚ��������룬����������Ӧʱ�����Ӽ�������ҩʱ�ɲ裬��������������������ܱ����ա�
����������ߵĹ�����Ѫ�����������ģ�ͬʱ���ԭ�е����س�Ѫ�Ѿ�ֹͣ���������ƶ�һ�㲡�˵���ЧѸ�ٶ����ԡ�������Ч����������Dz����Ծ�֢״������ת����ʼ���ƺ��ʱ������֯��ϸ�������������ߣ�����5��10���ﵽ�߷壬ƽ��6��8������Χ2��16���������Ժ��ֽ���������Χ�ڣ�Ѫ�쵰�׳������ƿ�ʼ���ܺ����������ͬʱʳ��������������ǿ����ɫ��ת������֢״����������������ʧ��Ѫ����ȫ�ָ���������Ҫ������ʱ�䡣����ʹѪ�쵰������ȫ������С�������������Լ���3��6���£��Բ�������Ӧ�е�����������
����ά����C���ܴٽ�ʳ�����������գ�������������ʱ���DZ�Ҫ�������ܴٽ����������գ��������ٽ����������գ��ʿڷ���������ʱû�б�Ҫͬʱ����ϡ���ᣬ���Dz�����ȱ�����θ����֢״���б���ά����B6����߹�����������ã�����Ϊ1.5mg/kg/�գ������οڷ���
��������ڷ����β���ʹƶѪ���ᣬ�뿼�����п��ܣ��ٲ���δ��ҽ����ҩ��������ƶѪ���ܲ���ȱ���Եġ�����������۳�Ѫδ�õ�������ʧѪ�������������ɵ�������ͬʱ������֢����Ⱦ�����������ȼ��������˹�����������ã����и�к���䶯���٣�Ӱ�����������գ�������ҩƬ�¾ɣ�������θ�����ڲ��ܺܺ��ܽ⼰���ա�
����������ע��������һ�㾡���ÿڷ�ҩ���ƣ�������������²�Ӧ��ע���������ٳ������������ղ���������θ�г���θ���Ǻ��������Ը�к��֬�����ȣ���θ�������������ڿڷ�������֢״���أ��������������������Խ᳦�ס��ڶ��Խ᳦�ס�θ�г���θ���������Ҽ�����ʱ����Ż�µȣ��ۿڷ������侭��������������θ������Ӧ��
�������õ���ע�����������������ɽ�洼�����������������Ƽ�������50mg/ml���������ܼ���Ӧȷ���㣬��Ӧ�������������������ж������㷽����ÿ���Ѫ�쵰��10g/L(1g/dl)������������������ɽ�洼��������300mg�������ﵽѪ�쵰��150g/L(15g/dl)������������500mg���㣬�����ܼ�����mg����300����15�����˵�Ѫ�쵰��g/dl����500���״θ�ҩ��Ϊ50mg����������Ӧ���ڶ��տ�����100mg������������Ӧ���Ժ�ÿ��100mg��ֱ���ܼ������ꡣ��ҩ;�����λ����ע�䡣��������������ϡ�ͺ���������ע��������������Ӧ�������ƹ㡣
����Լ��5���IJ���ע��������ɷ����ֲ���ʹ��ͷʹ�����ȡ�ݡ����ȡ���������������ע���Ӧ������ء�
�����������������ơ���ǿӪ�������Ӻ����ḻ��ʳƷ��Ѫ�쵰����50g/L(5g/dl)ʱ����Ѫ���ϸ����Һ�������Ĺ��ܲ�ȫʱ���˶��������Ѫ�����ٶ�Ҫ�����Է������������
����Ԥ��
����ȱ����ƶѪ����ǿ���Ԥ���ģ�����������ƶѪ����Ⱥ��Ӧ���ӿ�չ�������̺Ͳ�ȡԤ����ʩ�����磺�ٸĽ�Ӥ���IJ��鷽������ʱ�����ʵ��ĸ���ʳƷ���ڻ����᳹�ƻ���������ֹ����������ܣ�����������ںͲ����ڼ��ÿ�տڷ���������0.2��0.3g�����ڹ��没���е������д��ģ�ļ����没���ι������ݼ�ʱ�������Գ�Ѫ�
�����ϰ���ƶѪ��Aplastic Anemia��
���������ϰ���ƶѪ��������ϣ���һ�ֶ��ܸ�ϸ��������������Ϊ��Ѫϸ��ȱ����������Ѫ��֯��֬����֯�滻������ѪҺ��ȫѪϸ�����٣��ٴ��ϳ����ֽ��ص�ƶѪ����Ⱦ�ͳ�Ѫ��
����������һ�ֱȽϳ�������Ѫϵͳ����������Ŀǰ��ȱ��ȫ����飬���ݽ������ƽ��ɽ�кͺ�����ĵ�����������ղ������䷢�������˿��зֱ�Ϊ1.87/10��2.1/10��������׳��ռ������������Զ���Ů�ԡ�
��������
����Լ�������ϲ������Ҳ������ԵIJ���Ϊԭ�������ϡ����ֲ�����Ȼ���ڻ�ѧ���������������ضԹ���Ķ������������𣬳�Ϊ�̷������ϡ������ԭ����ҩ�ù�ҵ�������нӴ�����ѧ���ʵ��ж������������Ǹ�����ʽ�ĵ�����䣬���ټ��IJ�����Ⱦ�����߷�Ӧ�ȣ���5��2��5����
��5-2-5 ���ϵIJ������
| ԭ���� |
| �����ԣ�������ƶѪ��Estren-Dameshek anemia�� |
| ����� |
| �̷��� |
| ��ѧ���غ��������� |
| ҩ�� |
| ��ҩ��Ļ�ѧ���� |
| ������� |
| ��Ⱦ |
| ���������ף�Epstein-Barr |
| ϸ����������� |
| ��л |
| ������ |
| ���� |
| ���� |
| ��Һ���� |
| ϸ������ |
| ����˯����Ѫ�쵰���� |
| ���������쳣�ۺ������������Թ��������쳣�� |
��������̷������ϵ�ԭ�����£�
����һ��ҩ�P��ѧ���ʡ�
�����������ʸ��������ÿɷֳ������ࣺһ���붾��ļ����йأ�ֻҪ���Ӵ��ļ����ϴ��κ��˾��ܷ������������ϰ����絪�桢����������6�������ʡ��������ȿ�����ҩ���һ�����ڽӴ������Ƽ�����ҩ���һ�����ʱż������ijЩ�����������ϣ����ȣ��ϣ�ù�ء���̩�롢�ǰ����ҩ������ر�ֵ������ȣ��ϣ�ù����ҩ�����������������IJ�����������ҩ��������йء�����ҩ����һ�ֵ���������ڶ�������£��������Ƶij̶���ҩ������йأ���������ڿ����ԵĹ������ơ��������������ϸ����������ĵ��ϳ��ܵ������ƣ�ͣ��ҩ��������Ƴ��ɻָ����ں���������£�������ԼΪ1/2��4���1/20������������ҩ������أ��ƺ���һ�ֶ�ҩ��������Է�Ӧ��������һ������ø��ȱ�ݵ��º���ϳ���ȱ�ݣ�Ҳ������һ�ֹ�����Ӧ������ʹ��ҩ����ֹͣ�Ӵ������صĹ��������Գ��ڳ������ڣ���̩��Ҳ���������ϣ���ҩ��������أ��䷢�������������ù�ء�
�������ǹ�ҵ�û�ѧ��Ʒ����;��㣬Ҳ������Ҫ�Ĺ������ƶ��������������������أ�������һ�������Է�Ӧ�����������뱽ÿ��Ӵ���һ�δ�����Ӵ���Σ���Ը���ż�������뱽��ֹͣ�Ӵ���������������ų��ֹ�����������
��������������䡡
�������ֵ��������X�ߡ�������ͬλ�صȳ���������Ѫ��ϸ������������Ѫ������Ӱ���ϸ������ֳ�ͷֻ������˳̶���Ӵ��˷�������йء�
����������Ⱦ��
�������Ͽ��Է����ڲ����Ը���֮�ס��Ҷ��������²���Լ10��20�����Ỽ����ȫѪϸ������6����ǰ�и���ʷ�����ֲ��������Ƚ����ء�ͨ����Ϊ�йصIJ�������Ӱ����࣬����Ӱ����裬��νԭ�������ϲ����в�������ǰ���в����Ժ�������Ⱦ��
�����ġ�������
�������Ͽɷ���������ʱ�������ƶѪ����⡣���귢�����������ϲ��˵ĺ�ϸ���Բ������У�Ҳ��������˯����Ѫ�쵰������������ݱ�ɵ��͵����ϡ�
������������
�����������Ѫϸ��ȡ�������㹻�������������ĸ�ϸ������ϸ�������ܷ���������ֳ�����Ա�����㶨������ͬʱ�����������졢��ϸ����ϵͳ�ֻ����Ӷ������γɴ�������Ѫϸ����
������ϸ��ȱ�������ȱ�������ϵ�ԭ�����������ϻ��ߵĹ�����Ѫ��ϸ��������ʾ��������ϸ�����٣���ʾ���ܸ�ϸ�����ٻ�����ϰ������������ϰ���ƶѪ���߹�����ֲ�ɹ�����ʾ�����ȱ���ܹ�ͨ��ֲ�����������ϸ������������ˣ���ϸ��ȱ����ȱ��������ƶѪ�����ԭ��
�������ܸ�ϸ�����ض���������������ֳ���¡������ϰ���ƶѪҲ�������ڹ�����Ѫ����ȱ����ɡ�ʵ�����������ʻ�������Ѫϸ����ֳ�ͳ����е���Ҫ�ԡ�����Ǵ���������������ϸ���㣬�����ڳ��������и�ϸ������������������ֲ�ɹ���ų������쳣���������ĸ�ϸ���ǿ���ֲ�ģ���������ȱ�ݵ�����ϸ�����ܲ�������ȫѪϸ�����٣����;�������
�����������ϸ���ܹ�������Ѫ�������ӣ���GM��CSF�ȣ�������Щ��Ѫ�������ӹ�����ϸ����������ʱ������Ѫ�����ӣ���Ѫ�����еļ���̼����ӡ��ٺ�ϸ�����������ӣ������ϵķ������ܲ���������Щ���ӵļ��١�
��������Ҳ������ϸ������Һ���߶���Ѫϸ�����ƵĽ����������ע������������Ѫϸ�����������ơ����ÿ��ܰ�ϸ��Ѫ���������ϻ�óɹ�����ͬ��˫̥��ֲ�г�����Ҫ�����������ƣ�ֻ��50��ͬ��˫̥���ϻ��߹�����ֲ��óɹ�������50��ֻ���������ƽ���Ԥ�������ܳɹ�����֤��������T�ܰ�ϸ�������Ƹ�ϸ���������ͷֻ�������Ҳ�������ɿ���ϸ���������Ѫǰ��ϸ���������¡�
���������ϰ���ƶѪ����������˵�����˽����ܸ�ϸ������Ѫ���������߷�Ӧ֮��Ĺ�ϵ������Ϊ�����ӡ���seed��������������soil���͡����ӡ���worm��֮��Ĺ�ϵ�����ܻ�Ҫ�ӡ����ϡ���Fertilizer�����⼸�ֳɷ��У�������һ�ɷ�ȱ�ݶ��ᵼ�����ϵķ�����
�����ٴ�����
������Ҫ���ٴ�����Ϊ������ƶѪ����Ѫ����Ⱦ����������Ѫϸ�����ٵij̶ȼ���չ���ٶ��йء�ƣ��������������Ƥ��ճĤ��ƶѪ֢״��Ƥ����ճĤ���㼰���ߡ�������Ѫ��������Ů�Ի������¾����ࡢ���п�ǻ��������Χ��Ƥ�����Ϻ����ȸ�Ⱦ֢״��һ�����ܰͽ��Ƣ���״�����Ⱦ�����ڶ����Ѫ���ʹƢ������״�
�����ҹ�ѧ�߽����Ϸ�Ϊ���ͣ�
����һ�������͡�
�����������ᣬ֢״���أ�����ͻ����֢״�Ǹ�Ⱦ�ͳ�Ѫ�����ȡ�η������������ǻ���ʲ�����Ƥ����Ⱦ�������϶�������߿����Ѫ֢��������Ƥ�����㡢���ߡ�������������Ѫ����������Ѫ��Ů���¾�����ȳ�Ѫ֢״�϶�����۵ɳ���С��Ѫ�㡢��Ѫ�����״��Ѫ���ڳ�Ѫ��ټ���������������֮��Ѫ��λ�ȶ࣬�̶���������ء�ƶѪ�ڲ�֮���ڽ��ᣬ�����н��٣�������ȸ��ס���Ƣ���״����ಡ�������ն��̶̴٣�һ�㳣�����Ʒ�����Ч�����ѡ����ߴ����������һ����������
�������������͡�
����������컺����Ҫ�ı��ֳ����Ǿ뵡���������ۺ����١��ļ¡�ͷ�Ρ���ɫ�ס����г�Ѫ������������Ѫ���ټ�����Ⱦ������һ����������ֽ��������ƺ�����ơ��Ρ�Ƣ�ܰͽ�����״����ڲ���ż��Ƣ������״��̽ϳ������߿���������꣬������ת�����ӽ�Ȭ�������ֻ���ת��Ϊ�����͡�
����ʵ���Ҽ��
����һ��Ѫ��
����ȫѪϸ������Ϊ����Ҫ���ص㣬����ϸ������ϸ����ѪС��ļ��ٳ̶Ȳ��ȡ��Ҳ�һ��ͬʱ���֣�ƶѪ����ϸ����ɫ�ԣ���֯��ϸ���ٷ������������������Բ�����ʱ����������ߣ�������������������Լ��ͣ�����Ϊ25��100��109��l .2.5��1010��ul������ϸ�����������٣�������ϸ�����٣���������Լ��ٵ����������ø�������ʺͻ��־����ߡ��ܰ�ϸ���İٷ������ߣ������������ز���Ҳ�Ǽ��ٵģ�����ϸ��Ҳ���١�ѪС��������٣����г�Ѫʱ���ӳ���Ѫ�����������������������ԡ�
��������������
�������Բ����Ĺ��贩�����й���С�����٣�֬������Ȼ���࣬���£������������ͻ��ضȼ��ͣ��к�ϸ���������٣���Ҫ��������ϵϸ�����٣���ϸ�����ٻ���ʧ���ܰ�ϸ���������࣬����Ѫϸ���罬ϸ������֯ϸ������֯�ȼ�ϸ�����ࡣ
���������Բ������ȡ������������λ�Ĺ��裬�ɳʹ���������Ծ����ϵ����ϵϸ�����ٲ�һ�������ԣ������������࣬����ϸ���Լ��٣�һ�����Բ���Ӧ�öಿλ���贩�̣�ͬʱ�������졣
�������������졡
���������첡����Ƭ����Ѫ��֯�������٣�������֬����֯��������ܰ�ϸ������ϸ������֯ϸ���ֲ������ɵļ����С�
�������
�������������Ҫ�����ٴ����н�����ƶѪ����Ѫ����Ⱦ֮���֣�ȫѪϸ�����٣���֯��ϸ�����٣����ܳ�����������ѪҺ�����ı�����������������ȷ��ע��Ѱ�ҿ��ܵķ������ء�
����1987��6���л�ѪҺѧ����Ľ������ϰ���ƶѪѧ���������������ϰ���ƶѪ����ϱ���
����һ��ȫѪϸ�����٣���֯��ϸ������ֵ���١�
��������һ����Ƣ�״�
����������������ʾ����һ�����������ͻ��ضȼ��ͣ���������Ծ�����о�ϸ�����٣�����С���ɷ���Ӧ������Ѫϸ�����࣬��������Ӧ�������죩��
�����ġ��ܳ�����������ȫѪϸ�����ٵļ�����������˯���Ժ�Ѫ�������������쳣�ۺ����е�������ƶѪ��������Ѫ����ͣ�ͣ�������ά��������Ѫ����������֯ϸ�����ȡ�
�����塢һ�㿹ƶѪҩ��������Ч��
�������������ϰ���ƶѪ��Acute Aplastic Anemia AAA��������������ϰ���ƶѪ�����ͣ�Severe Aplastic Anemia-��,SAA-����ϱ���
����һ���ٴ���
������������ƶѪ�ʽ����ԼӾ磬�������ظ�Ⱦ�������Ѫ��
��������Ѫ��
������Ѫ�쵰���½��ٶȿ��⣬��߱���������֮�������֯��ϸ����1��������ֵ��0.015��1012/L(<1.5��ul)���ڰ�ϸ�����Լ��٣�������ϸ������ֵ��0.5��109��L����500/ul������ѪС�壼20��109��L����1��2��ul����
��������������
�����ٶಿλ�������ͣ���ϵ��Ѫϸ�����Լ��٣�����Ѫϸ�����࣬��������Ծ�����ܰ�ϸ�����ࣻ�ڹ���С������Ѫϸ����֬��ϸ�����ࡣ
�������������ϰ���ƶѪ��Chronic Aplastic Anemia CAA����ϱ���
����һ���ٴ���
������������ƶѪ����Ⱦ����Ѫ���ᡣ
��������Ѫ��
����Ѫ�쵰���½��ٶȽ�������֯��ϸ������ϸ����������ϸ����ѪС��ֵ�ϼ��������ϰ���ƶѪΪ�ߡ�
��������������
��������ϵ����ϵ���٣�����һ����λ�������������������ã���ϵ�г������죨̿�ˣ��������ࡢ��ϸ�����٣��ڹ���С��֬��ϸ��������Ѫϸ�����ӡ�
�����ġ��������粡����ٴ�Ѫ�������뼱�������ϰ���ƶѪ��ͬ��
���������������ϰ���ƶѪ�����ͣ�Severe Aplastic Anemia-��SAA-��
�����������
���������ٴ������������ȫѪϸ�����ٵļ�������
����һ�����Էǰ�Ѫ��Ѫ����
������������ƶѪ����Ѫ����Ⱦ�����иΡ�Ƣ���ܰͽ��״��ع�ѹʹ����ϸ���������ͣ�ѪƬ�к��ٻ���ȫ�Ҳ���ԭʼ�����ɰ�ϸ������������ԭʼ���ܡ����ˣ�ϸ���������ࡣ
������������˯����Ѫ�쵰����
�������������ں�ϸ��Ĥ�ṹ�ı��죬�Բ����ر����ж������һ�ֻ��������Ѫ������Ѫ����ʷ��˯��ʱ����֮Ѫ�쵰����������Ѿ�ɫ���������ڲ�����Լ��1/4��1/2�Ļ��߿ɲ������ϣ���ʱ������ʾ�������Ͱ�ȫѪϸ�����٣��ٴ��ϳ�Ϊ�����ϰ���ƶѪ������˯����Ѫ�쵰�����ۺ����������߹�ϵ���У����ʱ�����������˯����Ѫ�쵰��������ʱ����֯��ϸ�������⣬�й���Ѫ�������ữѪ����Ѫ���顢������Ѫ���顢���к���Ѫ��������ɳ����ԣ���������������ϸ����������ø�������Խ��ͣ�������ȴ���ߡ�
��������������ֳ�쳣�ۺ�����MDS����
����������һ�鲡�����Ĺ�����Ѫ��ϸ����Ѫ�����쳣��ѪҺ����������Ϊ����Ѫ��һϵ���ϵѪϸ���������٣�һ�㿹ƶѪ������Ч������������Ծ�����Ի�Ծ�������к졢���;�ϵ������̬�쳣���ɼ�С��ϸ������������ꣻԤ����������ĩ�ڶ�ת��Ϊ���Է��ܰ�ϸ����Ѫ����������ƶѪ����Ѫ���Ⱦ������
������������������ǵ������Ĺ��������쳣�ۺ�����������ϵ�о�������ͻ���������ϸ������ϵ��Pelger-Huet�˸ı��Bull/-eye myelocyte��ѪС������쳣��ѪС�������Ѫ����ƣ�ϸ���Ŵ�ѧ�����������ϡ�
�����ġ�������֯ϸ������
����������ȫѪϸ�����٣���������ٸ��ȣ��ڸΡ�Ƣ���ܰͽ��״۹��������쳣��֯ϸ�����������б�
�����塢������Ѫ����ͣ�͡�
��������������Ѫ��ƶѪ��������������и�Ⱦ���յĻ����з�����ȫѪϸ�����٣���֯��ϸ���ɽ���0���������ϸ��ϵ���٣����������ϡ����ڲ������ڹ�����־�ԭʼ��ϸ����������һ�������Լ�����Ԥ�����ã�������������
��������Ӫ���Ծ���ϸ����ƶѪ��
����������Ӫ����������ʷ�������Ե�������֢״��Ѫ��Ϊ��ϸ����ƶѪ��������ϸ���˷�Ҷ���࣬����������Ծ�����ֽ϶����ϸ����Ѫ��Ҷ���ά����B12ֵ���ͣ���Ҷ���ά����B12����Ч�����á�
�����ߡ�Ƣ���ܿ�����
��������ѪȫѪϸ�����٣���Ƣ�������״���������Ծ��
��������
����һ����ֹ�붾��Ӵ���
��������Χ�����з��п���������������ʾ�Ӧ��ȥ�����Ӵ�������һ�жԹ����������õ�ҩ�
��������֧������
������һ�����Ӹ��˺���Χ�������������������Ƥ����࣬�ÿ������������͵��굶�����ӿ�ǻ������������ˢ�ʹ��������������ע�䡢���̾�Ӧ�ϸ�������������������ϸ�������ر���ߣ�������ϸ����500��mm3��0.5��109/L��������롣
���������������Ƹ�Ⱦ��Ԥ����Ⱦ��Co-SMZ���ɼ��ͳ�ϸ����Ⱦ�Ϳ��Ϸ��ҳ���ķ����ʡ����Ƹ�Ⱦ�ɸ�����ע��ϸ������Ҫ�������ǿ����أ�Ӧ������ϸ��������ҩ�������飬ѡ����Ч�Ŀ����ء��緢�ȶ������Ⱦ��ϸ����δ���������Ȳ��ô�������������簱����ù�ء����ù�ؼ������ȷ�ù�صȡ�
����������ֹѪ��������Ƥ�ʼ����м���ëϸѪ��ͨ�Ե����ã���Ƥ�����ڡ��dz�Ѫ��ֹѪ���ýϺã��������ҩ7��10����δ��Ч��Ӧ��ֹͣ����ʹ�ã��������»���ɢ��Ⱦ���ڳ�Ѫ�����������������Ѫʱ����ø���������Ũ����ѪС�塣��ѪС�壬��ͬ������������Ч���ܿ���ͣ�����Ϊ��Ч����ͬʱ�����Ƽ����ı�������ע���ɻָ�ѪС�幦�ܡ�����������ӹ���Ѫ���ɸ�����غ��ͪ��ÿ��50mg����ע�����¾�����ǰ10�쿪ʼ�����¾�����ʱͣ�ã����رdz�Ѫ��ֲ�������
�������ģ���Ѫ����Ѫ��������һ����Ҫ��ʩ������Ӧ���ã���Ѫ����Ҫ��Ӧ����ƶѪ�������ߡ�Ѫ�쵰����60g/L(6g/dl)�����߲�����Ѫ�������Ѫ��Σ���Т����Ӵ�Ⱦ�����Ը��Ļ���������Ժ���Ѫ��Ӧ�Ļ�������Ӷ���ֲ��HLA�����߷�Ӧ��ʹ�Ժ������Ҫ������ֲʱ�ɹ��Ļ�����٣����������Ѫ��ɷ�������Ѫ��ɫ�س���֢������Ѫɫ������ɸκ����ٻ����ϰ���
���������̼�������Ѫ���ܵ�ҩ�
��������ҩ�����������̼��������Ѫ���ܣ��������Ч��ĿǰӦ���������ۼ��ء�
������һ���ۼ��ء����Լ�������ԭ��Ϊ���ٿ�ʹ�ٺ�ϸ�������ز������࣬��ʹ����Ѫ�쵰�ϳɣ���ֱ�Ӵ�ʹ��ϸ����G0�ڽ���G1�ڣ������ϸ���Ժ�ϸ�������صķ�Ӧ������ҩ��Խ�������Բ�����Ч�Ϻã��������Ͳ�����Ч������غ��ͪ�����˼���Ϊ50��100mg��ע��ÿ��һ�Ρ�������ҩ4���£����ⲡ����Ѫ�쵰�ָ��Ϻã���ϸ����֮��ѪС�峣���ܽӽ���������������ë�����ࡢ���Ů��ͣ�������ٷʴ��������ơ��鷿��С�����������������β�����ע�䴦��������Ӳ�顣
�����Ǽ���ͪ��Oxymetholone�������Ǽ���ͪ��Fluoxymetholone�����ü���Ϊÿ��100mg�ڷ�����������stanozolol����ÿ��6mg����3�οڷ�������ҩ����Ч�ϸߡ����Կڷ����������ᡣ���Ըι��������������о���Ҫע��ι�������Ľ����
����������������Ƥ�ʼ��ء������������ƺ�ƶѪ���ᣬ��������Ч�������ԡ�������������Ϊ������Ƥ�ʼ��ؿ�������֢���������Ӷ����ƹ���ѭ����ͬʱ�������߷�Ӧ�������ڸ�ϸ���������뷢����ǿ����ÿ��20��40mg�������οڷ������������ü�ǿ��������methylprednisone������ÿ��1g������Ϊһ�Ƴ̡�����ʵ�ʱ�����õڶ��Ƴ̣��ݳƴ��Ʒ���һ������Ч��
����������������������������ʿ������һҶ��̼��ﮡ��Ȼ��ܡ������ء�ݹ����ҩ��ĵð���ͭ�����ס�̥����ע��ȫ��ע��Һ�����������С�
�����ġ��������Ƽ���
��������������ϸ���ף�ATG����15mg/kg/d���ӵ�������5mg���������Σ���ͬʱǿ����ÿ��1mg/kg���ڷ�����5�죬���貿�ֻ���ȫ�ָ��ɴ�40��60����ATG�ĸ���Ӧ��Ѫ�岡����ߡ����ȡ���ս���ؽ�ʹ����Ĥ�ס�ѪС����ٵȡ�10���������ڿɷ�����Ѫ�쳣������˯����Ѫ�쵰����Ͱ�Ѫ���ȡ����������û��߾���A(Cyclosporine CSA)�ߣ���SAA��һ��Ч����
�����塢��ҽ���ơ�
������ҽ��Ϊ�������ڡ�����Ѫ�顱��������Ѫ��������ҽ���ۣ������ǣ������裬�������˴Ӳ������֣����б�֢ʩ�Ρ�
��������Ƣ�г���
����һ���˵��Ƣ�г����ܸ��ƹ������Ѫ���ܣ�����ϸ���ƻ�����ΪƶѪ��Ҫ����ʱ��Ƣ�г���ƶѪ���ɼ��ᣬ��Ѫ�������١�Ҫ����ѡ�������������������̶��кã�����Ѫ�ɷ֣���Ѫ���ͻȻ���̣����ü���������ʱ��Ч��������δ���ת�ߣ���ѡ��Ƣ���Ʒ���
�����ߡ�������ֲ��
����������ֲ���������������ϲ��ˣ�������ã�δ����Ѫ��δ����Ѫ�߹�����ֲ���Ϳ��������ɴ�80�������ѽ��ܶ����Ѫ�������½���40��50��������δ������Ⱦ��������30�������ߣ�Ԥ�����û�������������ȫ�����䣬��������Է��Ͱ����ϡ���MTX��CyclosporineԤ����ֲ����������GVHD����˫��̥֮��Ĺ�����ֲ����һ�β�����Ԥ���������һ��ʧ�ܺ��������Ƽ�Ԥ�������еڶ��ι�����ֲ���ɻ�óɹ���
�����ˡ���Ѫ�������ӡ�
������Ϊ���蹦��ȱ�ݣ�ѭ���дٺ�ϸ��������ˮƽ�������ߣ��������˴ٺ�ϸ�������ضԱ������Ƶļ�ֵ�������ɡ�GM��CSF��IL��3����ϵ�;�ϸ������ϸ�������ã���ʹ��Ҳ�����м�ֵ,��ǰ�ٴ����ñ��������ϵ���Ч����������ʱ�ġ�
����Ԥ��
����һ����ֹ���ö���Ѫϵͳ����ҩ��ر�����ù�ء���̩�ɵ�һ��ҩ�����ʹ��ʱ����ǿ�۲�Ѫ��ʱ��ȡ�ʵ���ʩ��
�����������ڽӴ������𱾲��Ļ�ѧ���������ص���Ա��Ӧ�ϸ�ִ�з�����ʩ���ϸ����ز�����̣���ֹ�к��Ļ�ѧ�ͷ�����������Ⱦ��Χ������
Ӫ���Ծ���ϸ����ƶѪ��Nutritional Megaloblastic Anemia��
��������ϸ����ƶѪ������Ҷ�ᡢά����B12ȱ��������ԭ������DNA�ϳ��ϰ����µ�һ��ƶѪ������ƶѪ�Ĺ�ͬ�ص�������Ѫ�ʴ�ϸ����ƶѪ�������г��־���ϸ����
�������ҹ�����Ҷ��ȱ�����µľ���ϸ����ƶѪ����ɽ�������������ϡ�ɽ���ȵرȽ϶����ά����B12ȱ�������ߺ��ټ�������ƶѪ��Ϊ������
����Ҷ�ἰά����B12�Ĵ�л��
����Ҷ�ἰά����B12�Ĵ�лҪ�����5��2��6��
��5��2��6 Ҷ�ἰά����B12�Ĵ�л
| �� | Ҷ�� | ά����B12 |
| �����Ϸḻ��ʳƷ | ������ɫ�߲ˡ�ˮ�����ϡ����ࡢ���ࡢ�Ρ����� | ���ࡢ�Ρ������ĵ����ࡢ�ݵ����飨�߲��м��٣� |
| �����κ�ɥʧ | 50��90�� | 10��30�� |
| ����ÿ����Ҫ�� | 50��100ug | 2ug |
| ���ղ�λ | ʮ��ָ�����ճ� | �س����������ӽ�Ϻ� |
| ���������� | 5��10mg | 2��5mg |
| ÿ�������� | 50ug | Լ2��5ug |
| Ѫ������ֵ | 13.62-45.4nmol/L(6-20ng/ml) | 148��666pmol/L(200900pg/ml) |
�����߲ˡ�ˮ������ʳ��������Ҷ�����Դ������ʳ���кܴ�Ҷ��ɱ������ƻ�������ÿ�����Ҫ����������50ug�����������Ⱦ�����ȵȴ�л���ߵ�����£���Ҫ���ɱ���������¸�����Ҷ������ղ�λ��ʮ��ָ�����ճ��ϲ���ʳ���еĵ��Ȱ�����˹��ϳɵ�Ҷ�ᶼ���ױ����գ���ʳ���еĶ�Ȱ���Ҷ��ۺ�����뾭øˮ��ɵ��Ȱ�Ҷ�����ܱ����ա��ڳ�ճĤϸ����Ҷ�ᾭ����ԭ���������ɵ��Ȱ�������Ҷ�ᣬ��Ѫѭ�������������֯����Ҫ�����ڸ����ڣ�ȫ����Ҷ������������Ϊ5��10mg������ÿ���������Ƚϴ������ʳ����ȫ����Ҷ�ᣬԼ4����ʱ�伴��ʹ���������ص�Ҷ�ᶼ�����ꡣ����Ѫ�庬��Ϊ13.62-45.4nmol/L(6-20ng/ml)��
�������岻�ܺϳ�ά����B12��������ϸ�����ܺϳɣ����ֺϳ��ڴ��ӷ�����ų������ܱ��������á��������ά����B12����Դ��ȫ����ʳ�����ĸΡ������ġ��������֯���ݵ����鼰��Ʒ��ά����B12��ḻ����Դ���߲��к������١�ά����B12ÿ�����Ҫ������Ϊ2ug��ʳ����θ������ʱ��ά����B12���ͷų�������θ�岿��ϸ�������ڵ������ӣ�һ���ǵ��ף���ϣ�����Է�ֹά����B12���ƻ�����ʹ�䱻�س�ճĤ���ա�ά����B12������ʱ��ת�ܵ��ע��ϵ��Ժ�����һ���ǵ���ת�ܵ��ע��ϣ���Ѫѭ���������ࡢ���輰��������ֳ�е�ϸ��������ά����B12����������Ϊ2��5mg������Լһ�������ڸ����У�����ÿ�����ļ��٣�2��5ug������������������������������ģ���ʹʳ���г���ȱ��ά����B12������ҲҪ����3��6����ܳ�������ά����ȱ������������Ѫ����Ϊ148��666pmol/L(200-900ng/ml).
��������������
����Ҷ��ȱ����ԭ����:�����벻��,��ĩ�����߲��ٵļ��ڽ϶��,Ӫ��������ƫʳ��ʳ�����������Ҷ��ȱ������Ҫԭ�����ղ�������������к���ȴ������Ը�к������Ҫ���ӣ��������Ҷ����Ҫ������5��10���������顢Ӥ����������Ѫ��ƶѪ���������������������Լ�����Ҳ����Ҫԭ��֮һ���������ϰ���Ӧ��Ӱ��Ҷ���л�����յ�ҩ���簱����ʡ��Ұ���ड�����Ӣ�ơ������¡���˿����ȡ�
����ά����B12��ȱ����������θ�������������йأ���ʳ����ȱ��ά����B12�������ߺ��������ڳ�����ʳ����ż����ɷ���������������������ά����B12ȱ���Ļ����ɷ�Ϊ����ȱ�������ӣ��������ƶѪ��θ�г�����ȫθ�г�5��6���������ƶ��θ��ȫ�г�1�����;���ƶ��5���м��;���ƶ�����ڳ����ղ��㣬����㷺�س��г����ڶ���С���ס�����к���ȴ������Ը�к�ȣ��ۼ������ϸ������ά����B12������̶�Ҷ��ͷ�г没������������ä���ۺ����ȡ�����ƶѪ����ڱ�ŷ���壬�г没���µľ���ϸ����ƶѪ��ȥ����ڷ�������������ԭ�������ƶѪ���ҹ������ټ���
��������Ҷ���ά����B12����DNA�ϳɹ�������Ҫ�ĸ�ø(ͼ5-2-4)����DNA�ϳɵ�;�������������ת���

ͼ5��2��4 Ҷ����ά����B12��л�����ϵ����DNA�ϳɵ�����
����������ण���һ����������ļ����Ǽ�����Ҷ���ṩ����ˣ��κ�ԭ�������Ҷ��ȱ������Ӱ�������������̣����Ӱ��DNA�ĺϳɣ��Ӽ�����Ҷ��ת�������Ҷ��ʱ��ά����B12����һ����������������ã�ʹ������Ҷ��ȥ��������ת��Ϊ����Ҷ�ᣬ�Ӷ��ٽ�DNA�ĺϳɡ���ˣ�ά����B12ȱ��ʱ���Ӽ�����Ҷ��ת�������Ҷ�ἰ�Ǽ�����Ҷ��������٣�����ά����B12ȱ������ɵĽ����Ҷ��ȱ���Ľ����ͬ��ͬ��������DNA�ϳ��ϰ������DNA�ϳ������ͣ�Ѹ�ٷ��ѵ�θ������Ƥ����Ѫϸ������Ƥ��غ���������Ƥ�����ᷢ�����ױ䣬��������ά����B12��Ҷ��ȱ��ʱ��DNA�ϳ����ͣ�ʹ��ϸ������������DNA�ϳ����ӳ���ÿ��ϸ��DNA���������������ӣ���ϸ�����ѳٻ�����������RNA�������Ӻܶ࣬���ߵĺϳ�Ѹ�ٳ���ǰ�ߣ�Ѫ�쵰�ϳɲ������͡��ʳ��ֺ˽�������ƽ��֮����ϸ������������ϸ�����ڹ�����δ�����켴���ƻ�һ��ϸ����Ч���ɡ�DNA�Ĵ�л���ͶԹ�����ϸ������ϸ���ij���������Ӱ�죬��Ч��ϸ����ѪС�����ɣ��ʳ�����ϸ����ѪС����٣����־������������˺ˡ���ϸ����Ҷ���ࣩ������Ѹ����ֳ��ϸ�������ǻ��θ��С�����ӹ�������Ƥϸ�������ְ������˲����켰����������֢״�����⣬ά����B12�ܴٽ�����������øA��methylmalonyl COA��ת�����������øA��succinyl COA�������ά����B12ȱ�����˷�Ӧ���ܽ��У������ı�����COA��propiony COA���ѻ���propionyl COA��methylmalony COA��succinyl COA����Ӱ��֬����������ϳɣ�����֬�����Ͻ�֬Ĥ��Ӱ������Ĥ�Ĺ��ܣ�����ά����B12ȱ��ʱ������ϵͳ֢״��ԭ��
�����ٴ�����
����һ��������Ҷ��ȱ����ά����B12ȱ����ͬ�ı���Ϊ����ϸ����ƶѪ��������֢״����ά����B12ȱ�������Ƕ���ƶѪ���߿ɳ�����ϵͳ֢״��
����һ������ϸ����ƶѪ��
����ƶѪ�������أ���Ҫ�����ߡ�˥����������ƣ�롢�ļ¡����١�ͷ�Ρ��ۻ���������һ����ƶѪ��֢״�����ֲ��˿�����Ȼ��㡢Ƥ�����ڲװ�����Ȼ��㣬�ʳ���������ʻ�ɫ�����ƣ���
��������������֢״��
������ʳ������������ʳ���͡���к��Ż�¡����ء����ס���ʹ������ͷή��������⻬�������ࣩ������筺�����ţ������ţ���ࣩ�ȡ�
����������ϵͳ֢״��
�������͵ı���Ϊ������ָ�о��쳣����̸С���ľ�����д���о��ϰ�������������ǵڶ�ֺλ�ø�ɥʧ����������ʧ����һ����չΪ�����Թ���ʧ������������ͺ��������Ա��Ըı�������һ��Ϊ�Ǽ������ϱ��ԡ�վ������·���ȡ��췴������ϥ�켰���췴���������ʧ������ֺ���䣨Babinski���������������������ԡ�����Χ�ͼ����⣬ά����B12ȱ��ҲӰ����ԡ���˯��ζ����������Ӿ��쳣���մ���������������������ľ������֢��������쳣�Dz�̬���ң�����֢״�������١�
����ʵ���Ҽ��
����һ��Ѫ��
����ƶѪΪ��ϸ����ɫ�ͣ�ѪƬ�к�ϸ����С���ȣ����ξ������ԣ�������Բ�εĴ��ϸ���϶ࡣ��ϸ���пɼ���Cabot����Howell-JollyС�塣��ϸ����ѪС����������ȼ��١�������ϸ����Ҷ���࣬5Ҷ���ϣ�5��������߿���16Ҷ������������ʾϸ����˥�ϣ����ǰ��˷����쳣��Ⱦɫ�ʵ��쳣��ż������ϸ��������ϸ����˵�������ڸΡ�Ƣ��������Ѫ��
��������������
��������ϸ���ر��Ǻ�ϵ������������������ʽ��ͣ���ϵϸ�������Եľ���ϸ���ص㣺ϸ���������Ⱦɫ�ʳ�ϸ����״�����ɷ�ɢ���γ�һ������ļ�϶������֮�����Ȱ��˳��죬�γɡ������ϡ��������������������Чҩ�����ƺ�24��96Сʱ����ȫ��ʧ����ϸ��ϵͳ�;�ϸ��ϵͳ���������Ƶĸı䣬���־����������;���״����ϸ�������ͺͷ�Ҷ����ľ�ϸ�������������࣬�����ʵ����ƺ�ɼ��١�
��������θҺ������
����θҺ���������٣�����������ȱ�����������٣�ע���鰷������Ҷ��ȱ�����˿�����������������֣�����ƶѪ���ߵ�θ�������᳣��Զ��ʧ��
�����ġ�������顡
����Ѫ���ӵ����س�ƫ����ȳ���������Χ����Ԫ���ߡ�Ѫ����������ø��Ѫ������Ѫ�����������ߡ�Ѫ�����鵰�ס�����ͼ�������ø�����͡�Ѫ��Ҷ�����6.81nmol/L(3ng/ml)��Ѫ��ά����B12����74pmol/L(100pg/ml)��
�����塢�ǰ����Ȱ��ᣨformiminoglutamic acid FIGLU��
������й���飬��Ҷ��ȱ��ʱ��FIGLU��й���ߡ������Ǹ����˿ڷ��鰱��15��20�ˣ��Ժ�����е�FIGLU��������Ϊ9mg/24Сʱ��������FIGLU���ӣ���ʾ����Ҷ��ȱ������Ϊ�鰱���л��������Ҫ����Ҷ�ᣬ��Ҷ��ȱ��ʱ���������м��л����FIGLU�������ų���
��������������ά����B12�������飨Schilling���飩��
������һ���֣������߿ڷ��������ܣ�57Co��Co����ǵ�ά����B122�ˣ�ͬʱ����ע��ά����B121000�ˣ�Ȼ��ⶨ48Сʱ����ķ������á�ά����B12����������48Сʱ�����ų�����������ܵ�5��40����ά����B12������ȱ���ߣ������ƶѪ��θ��س��г����ȴ�Ӫ���Ծ���ϸ����ƶѪ����ķ������ò���5�����ڶ����֣�������սϲ�Ӧ�ظ����飬������ʱ������������ά����B12ͬʱ�ڷ������ų���ת��������ɽ�����ƶѪ���ȴ�Ӫ���Ծ���ϸ����ƶѪ���Լ���
������ϼ��������
��������ϸ����ƶѪ��ϵ���Ҫ�����ǣ���������֢״���ڵ��͵�Ѫ��ı����MCV��95fI����Բ�δ��ϸ�����࣬���ԵĴ�С���Ⱥ����Σ�������ϸ����Ҷ���ࣻ�۹����г��ֽ϶���͵ľ���ϸ���ȡ�����ϸ����ƶѪ����ϳ���������һ����ȷ��Ҷ��ȱ������ά����B12ȱ�������ݲ�ʷ��������ijЩʵ���Ҽ�鼰�������ƵĽ�������ۺϷ�������5��2��7��
��5��2��7 ά����B12��Ҷ��ȱ������
| �� | ά����B12ȱ�� | Ҷ��ȱ�� |
| ��ʷ | θ����������θ�������� | Ӫ��������ƫʳ�������Ѫ��ƶѪ�� |
| ��ϵͳ֢״���� | �϶�����������ϱ��� | �ټ���ĩ������ |
| ʵ���Ҽ�� | �� | �� |
| Ѫ��Ҷ��ֵ | ���� | <6.81nmol/L(3ng/ml) |
| Ѫ��ά����B12ֵ | <74pmol/L(100pg/ml) | ���� |
| B12����ʵ�� | �����ų������� | ���� |
| ��Schilling�����һ�֣� | �� | �� |
| ���������� | �� | �� |
| Ҷ�� | ��Ч | ��Ч |
| ά����B12 | ��Ч | ��Ч |
��������������ȱ�������������ʱ�����Խ����������ƣ����ж���Ҷ��ȱ������ά����B12ȱ��������Ҷ��ÿ��0.2mg��ά����B12ÿ��1ug��ע������10�졣�۲����Ʒ�Ӧ������֯��ϸ��������Ѫ�쵰�������ӣ�����ϸ����ʧ����Ϊ���Է�Ӧ����ʾΪҶ���ά����B12ȱ������Ϊ����������Ҷ��ֻ��Ҷ��ȱ���IJ�����Ч����ά����B12ȱ���IJ����������á�ͬ��������������ά����B12��ֻ��ά����B12ȱ���IJ��������á�
��������ϸ����ƶѪӦ����Ѫ֢���𡣺��Ѫ�����ߵĹ���������ֺܶ����ϸ�������������ж��ٲ�һ��ԭ��ϸ��������ϸ�����ж�˺��ش��ͣ�Ѫ��Ҷ���ά����B12�������١���Ҷ���ά����B12��������Ч����Ӧ����й�����������������������Ѫ�������������쳣�ۺ������������ϡ���Ѫ��ƶѪ���Ŵ�����������ȼ���
��������
����һ��ȥ��������²�ԭ��
��������һ�����ơ�
����������ƶѪʱ��������Ѫ�⣬һ�㲻��Ҫ��Ѫ����Ҷ���ά����B12���ƿ�ʼ��48��72Сʱ������Ч�������ؾ���ƶ���˿�ʼ���ƽΣ�Ѫ�ػ����½���Ҫ��ʱ���貹�䡣����Ӫ����
��������Ҷ��ȱ����
����Ҷ��5mg�ڷ���ÿ��3�Σ�Ҳ���ü�������Ҷ��3��6mg��ÿ��һ�μ�ע��һ������ҩ��ʼ��ĵ�5��10�죨8�죩��֯��ϸ����������������2�ܺ��ֽ���������Ѫ�쵰��ÿ2������20��30g/L(2-3g/dl)����ʳ���ӣ�������ʧ����1��2��Ѫ���������ȫ�ָ�������
���������Ҷ���ά����B12ȱ����ƶѪ��θ����֢״�ಿ����Ч�������ܼ�����ϵͳ֢״��������ʹ֮���ض�������صĺ������һʱ�ֲ���Ҷ��ȱ����ά����B12ȱ�����ɶ���ͬʱ���á�
����Ҷ��ȱ���IJ��˳�ͬʱ���е����ʡ�����ά���ػ�����ȱ����������ʱ��Ӧע�ⲹ�䡣
�����ġ�ά����B12ȱ����
������ά����B12���ƣ���ʼ��ÿ�ռ���ע��100ug��2�ܺ��Ϊÿ��2�Σ�������ҩ4�ܻ��Ѫ��ָ�������ÿ��ע��1�Σ���Ϊά�����ơ�����ƶѪ��ȫθ�г���IJ����賤�ڣ�������������ά�����ơ���֯��ϸ�����ߣ������ƺ��4��10�졣Ѫ�쵰��1��2���´����������Ѫ�������ʼ�����ԣ����Ժ����������Ӧ���Ǻϲ�ȱ����ƶѪ��Ӧ����������θ�����������ʧ�ڶ���ƶѪ���˳����ָܻ���������Χ������ת�ָ�����,��������ȴ������ת��
����Ԥ��
������ǿӪ��֪ʶ����������Ӫ��״���������Ժ�ά����B12��Ҷ��϶��ʳ�����ƫʳ���Ľ����ϰ�ߣ�Ӥ��Ӧ����ι�����и���ǿӪ����
��Ѫ��ƶѪ��Hemolytic Anemia��
������Ѫ��ƶѪϵָ��ϸ���ƻ����٣���������Ѫ���ܴ�������ʱ������һ��ƶѪ����Ҫ�����ܹ����Ӻ�ϸ�����ɣ����Դ�����ϸ�������������̣��ᷢ��ƶѪ������״̬��Ϊ��������Ѫ�Լ�����Compensated hemolytic disease����
��������
�������ݺ�ϸ���������̵�ԭ�ɷ�Ϊ��ϸ������ȱ�ݺ������������µ���Ѫ��ƶѪ��
����һ����ϸ������ȱ�����µ���Ѫ��ƶѪ��
�����������⣬����ȱ�����Ŵ��Եġ���Asby/�����������ĺ�ϸ��������ˣ���ϸ�������������������˵ĺ�ϸ����������ˣ����ϸ�����������̡�����ȱ�ݣ���Ѫ��λ����Ѫ���⡣
������һ����ϸ��Ĥ��ȱ�ݡ���ϸ��Ĥ�ṹ��ȱ�ݿ����Ĥ�Ŀ����ԡ�Ӳ���쳣�����ȶ����������顣�ڴ���������У�ȱ������һ�ֻ�һ�����ϹǼܵ��ף���ϸ����̬Ҳ�쳣����Щ�Ŵ���Ĥ�ļ����������Ŵ�������ϸ������֢���Ŵ�����Բ��ϸ������֢������˯����Ѫ�쵰�������ϸ��Ĥ�Բ����쳣���У�����Ĥ��ȱ����һ�ֻ���Ե��쳣��
����������Ѫ�쵰�ṹ������ȱ�ݡ�Ѫ�쵰�ṹ�쳣��ʹѪ�쵰�׳�Ϊ�����Ի��ȶ�,���º�ϸ����Ӳ�������Ѫ��������ϸ����ƶѪ���ȶ�Ѫ�쵰�ײ������к�ƶѪʱ��������鵰����������ʹ��ϸ����Ӳ���ƻ���������Ѫ��ƶѪ��
������������ϸ��ø��ȱ�ݡ�Ϊά��Ѫ�쵰��Ĥ���ϻ�������������ڻ�ԭ״̬��ά���㹻ˮƽ��ATP�Խ��������ӽ����ĺ�ϸ��ø��ȱ�����ɵ�����Ѫ��ƶѪ��ø�ļ����ɷ�Ϊ2�ࣺ�ٺ�ϸ�������ǽͽ���ø��ȱ�������ͪ�ἤø�����ں�ϸ������������·��ø��ȱ������������6��������ø����
����������ϸ������ȱ�����µ���Ѫ��ƶѪ��
�����ⲿ��ȱ�ݣ�ͨ���ǻ���Եģ���ϸ�����ܵ���ѧ�ġ���е�Ļ��������ء����P����ѧ���ص����˶�������Ѫ����Ѫ����Ѫ���ڣ�Ҳ����Ѫ���⡣
����������Ѫ��ƶѪ�ĸ�����Ҫԭ�����5��2��8
��5��2��8 ��Ѫ��ƶѪ�IJ���ѧ����
| һ����ϸ������ȱ�� |
| ��һ���Ŵ��� 1��ϸ��Ĥ�쳣���Ŵ�������ϸ������֢���Ŵ�����Բ��ϸ������֢�� 2����ϸ��ø�쳣�� ��1����ϸ���������ͽ���ø��ȱ������ͪ�ἤøȱ���� ��2����ϸ������������·��øȱ����������-6-��������ø��G6PD��ȱ���� 3��Ѫ�쵰�����鵰�����쳣�� ��1�������ṹ�쳣��Ѫ�쵰�ײ���������ϸ����ƶѪ��Ѫ�쵰��C��D��E�ȵĴ�����״̬�����ȶ�Ѫ�쵰�� ��2�����������쳣��������ƶѪ�����к�ƶѪ�� |
| ����������� ����˯����Ѫ�쵰���� |
| ������ϸ���������� |
| ��һ�������� ��1���¿����ͣ���2���俹���� 2��������ͬ�����ߣ�3��Ѫ�Ͳ�����Ѫ��4��ҩ���� |
| ��������е�� 1�����ഴ���ԣ�2��Ѫ�ܲ��ԣ�3���о���Ѫ�쵰���� |
��������ѧ����������������
|
| ���ģ�Ƣ���ܿ��� |
������������
������ϸ������ر��ƻ����Է�����Ѫ�����Ѫ���ڡ�Ѫ������Ѫ��extravascular hemolysis������ϸ����Ƣ�����еľ���ϸ��������һ����ϸ��ϵͳ�����ɺ��ƻ���Ѫ������Ѫ��intravascular hemolysis���Ǻ�ϸ��ֱ����Ѫѭ�������ѣ���ϸ�������ݣ�Ѫ�쵰�ף�ֱ�ӱ��ͷ���Ѫ����
����һ��Ѫ������Ѫ��
������ϸ���ھ���ϸ�����ƻ���Ѫ�쵰�ױ��ͷų��������ھ���ϸ���ڷֽ���鵰�ף�globin����Ѫ����(hematin),Ѫ���طֽ�Ϊ����һ����̼��̼��Ѫ�쵰�ף�Carboxyhemoglobin���������أ�biliverdin������������ɵ����أ�bilirubin����Ѫ���������ࡣ�ڸ��ڣ���������������ȩ����Ϊֱ�ӵ����ء�δ��������ȩ���ϵĵ����سƼ�ӵ����ء��������������ǽ��Ϊֱ�ӵ����ء�δ��������ȩ���ϵĵ����سƼ�ӵ����ء�������������ȩ�Ḵ���ᆳ��֭����С�����ֽ�Ϊ����ԭ������ԭ�ɱ�������ѪҺ���������ų���Ѫ������Ѫ�ɷ�����Ƣ���λ����ľ���ϸ����Ƣ��������Ч������������˵ĺ�ϸ��������Ƣ�����ж��ص�ѭ���ṹ������Ѫ��������Ƣ��Ѫ���������dz�ȥ�����ɹ㷺���˺�ϸ������Ҫ��λ��IgM�Ͳ�����������ĺ�ϸ�����������ڸ��౻��C3b����ĸξ���ϸ����ȥ����֮��IgM������û�в���ɷָ��ŵĺ�ϸ��������������������Ϊ����ϸ��û��IgG�����ĺ�ϸ�����ɼ������壬���ϸ������IgG���������ֻ��һ��������ӽ�ϡ���IgG�����ĺ�ϸ������ʹû�в���Ҳ�ܱ�����ϸ�������IgG�����ĺ�ϸ����Ҫ��Ƣ�౻����ϸ������IgG-Fe���壬����C3b���壩�����IgG�Ͳ������ͬʱ�����ĺ�ϸ���������Ѹ�٣���Ϊ���������ܶ�������鵼������Ѫ������Ѫ�IJ�λ�ͳ̶Ⱦ����ڿ�����������������ڡ��������ϸ������������쳣�ij����ǰ��ϸ����������Ч��ϸ�����ɣ�����к�ƶѪ�;���ϸ����ƶѪ���Ŵ��Ժ�ϸ��Ĥ��Ѫ�쵰��ϸ����øȱ�ݵȰ鷢����Ѫ��ƶѪ������һ���̶ȵ���Ч��ϸ�����ɡ�
��������Ѫ������Ѫ��
��������Ѫ������Ѫʱ��Ѫ�쵰��ֱ�ӱ��ͷ���Ѫ������Ѫ���еĽ���鵰�ף�haptoglobin���Dһ�֦�2�ǵ���һ��ϣ���������ӽϴʲ���������й������ϸ����ȡ������ɵ����ء���Ѫ�϶�ʱѪ���н���鵰��Ũ���������ͻ���ʧ������Ѫ���н���鵰��Ũ�ȵĸߵ�Ҳ�ܵ������������ص�Ӱ�졣
������Ѫ���ڽ���鵰��ȫ����Ѫ�쵰��Ϻ�����Ѫ�쵰�ֽ����Ѫ��������Ѫ���أ�hemopexin����һ�֦��ǵ��ף���ϣ�Ȼ��Ҳ����ϸ����ȡ��������ѪʱѪ��Ѫ���ص�Ũ���ཱུ�͡�
����Ѫ���е�����Ѫ�쵰�ױ������ɸ���Ѫ�쵰�ף�methemoglobin�����ٷֽ�Ϊ����Ѫ���أ�methematin��,Ȼ����Ѫ���а���ϳɸ���Ѫ����ף�methemalbumin���������Ѫ���ؽ�϶���ϸ����ȡ��Ѫ�����н϶������Ѫ�쵰��,Ѫ���ɳʷۺ�ɫ�������ڸ���Ѫ����׳���ɫ������Ѫ�쵰�׳ʺ�ɫ�������ۺ�ɫ���ڸǶ���������
������Ѫ���еĵ�������Ѫ�쵰�Ľ���Ѵﱥ��ʱ��δ��ϵ�Ѫ�쵰�����ڷ��ӽ�С��������66000�����������ڣ�ʹ��ɫ��졣����Ѫ�쵰����ɳ��������ڣ�ʹ��ʺ�ɫ������Ѫ��������ڷ��Ӵ����������ڡ�
��������Ѫ�쵰�ױ���С����Ƥ���պ�ֽ����������������Ѫ���ص���ʽ��������С����Ƥϸ���ڣ�����Ƥϸ������������ų�����������������軯��Ⱦɫ���ɼ�����Ƥϸ��������ɫ�ĺ���Ѫ���ؿ���������Ѫ��������������Ѫ������Ѫ��������˯����Ѫ�쵰����е����Ѫ��ƶѪ��
������ϸ���ƻ���Ѫ�쵰������һϵ�д�л�ı��ͼ5��2��5��
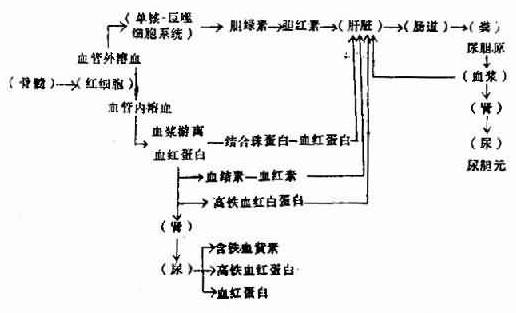
ͼ5��2��5 ��Ѫ��Ѫ�쵰�״�л��;��
�����ٴ�����
�������ݺ�ϸ���ƻ��IJ�λ��ͬ��ΪѪ������Ѫ��Ѫ������Ѫ�������͡�Ѫ������Ѫһ��ʼ�����Ѫ��Ҳ�ɱ���Ϊ������Ѫ���̣����������˯����Ѫ�쵰����G��6PDȱ�����俹����������������Ѫ��ƶѪ���Լ�ҩ���������Ⱦ����������֮��Ѫ��ƶѪ��Ѫ������Ѫһ���������Ѫ���̣�������Ŵ������κ�ϸ������֢��Ѫ�쵰�ײ����¿�����������������Ѫ��ƶѪ��
������Ѫ��ƶѪ���ٴ���������Ѫ�Ļ������̶Ⱥͳ����йء�
����һ��������Ѫ��
�������衢��ͻ����ս�����ȡ���ɫ�ס����ᱳʹ�����١������������ɳ��ֶ��ġ�Ż�¡���ʹ��θ����֢״���������ں�ϸ�������ƻ�����ֽ����Ի���Ķ����������¡�����Ѫ�쵰����Ѫ����Ũ��Խ��130mg%ʱ��������Һ�ų�������Ѫ�쵰������ɫ��Ũ����������12Сʱ��ɳ��ֻ��㣬��Ѫ��������С��ϸ������������Ѫ�쵰�׳�������С�ܣ��Լ���Χѭ��˥�������أ����¼���������˥�ߡ�����ƶѪ��ȱ���������߿ɷ�����־��Į����ԣ��ݿ˺��Ĺ��ܲ�ȫ��
��������������Ѫ��
�����ϻ��������������ס����١�ͷ�ε�һ����ƶѪ������֢״�������⣬���в�ͬ�̶ȵĻ��㣬Ƣ�����״���������ʯΪ�϶���IJ���֢���ɷ��������Ի��㡣��֫�ײ�Ƥ���������������ϣ�����������ϸ����ƶѪ���ߡ�
�������
������Ѫ��ƶѪ����Ͽɷֳ���������������ȷ������Ѫ��ӦѰ�Һ�ϸ���ƻ����ӵ�֤�ݣ��ڲ�����Ѫ��ԭ�����뾭����ʷ��֢״�������Լ�ʵ���ҵ����ϵ��ۺϷ��������жϡ�
����һ����ʷ��
������ѯ�ʷ�����������Ҫ֢״�Լ���������Ӧ����ѯ�����¸��
������һ�������ԡ�ǿ����ͥ���ᣬ����к�ƶѪ����ڹ㶫���������㽭���غ�������
��������������ʷ������������ƶѪ�����㡢Ƣ�״��ߣ�������������Ѫ��ƶѪ���ܡ�
����������ҩ��Ӵ�ʷ��ҩ����շ���������Ѫ��ƶѪ��������ҩ���ʹ���ȶ�Ѫ�쵰�ײ���G6PDȱ��֢������Ѫ��
�������ģ�������Ѫ��ƶѪ��ԭ����ʷ�����ܰ����ɰ�����������Ѫ��ƶѪ��
�������壩�շ����ء�����͡�����̼������϶��ȡ�
��������������
����Ӧע��ƶѪ���ƾҡ���Ƣ�״�ȡ�
��������ʵ���Ҽ�顡
�������Ŀ�ĺͲ����У�
������һ��ȷ���Ƿ�Ϊ��Ѫ��ƶѪ���ɸ��ݺ�ϸ���ƻ����Ӻ������������ǿ��ȷ����
����1����ϸ���ƻ����ӵ�֤��
������1����ϸ�������½���һ�����ϸ����ɫ����ƶѪ��
������2��Ѫ���ӵ��������ࡣѪ�嵨����Ũ�Ȳ�����������Ѫ�ij̶ȣ��������ڸ��������ӵ����ص��������ʻ���Ϊ��Ȼ��жȣ�Ѫ�嵨����һ����17.1-51.3ukmol/L(1-3mg/dl)���ң����ٳ���136.8umol/L(8mg/dl)�������㲻��ʱ���������ų���Ѫ��ƶѪ��
������3��������ԭ����й�����ࡣ������ԭ�����س����ӡ��ڸι��ܼ���ʱ�����������ظ������ӳ�������������ԭ��������ԭҲ�����ӣ��ʶ���Ѫ��ƶѪ����ϣ���ֵ���Ǻܴ�����ԭ�����ӵģ���������ԭ�Ķ����ⶨ�����Ѳ���������Ϸ���֮һ�����ڵ��������ԣ�����ͬʱ�������Ի��㡣
������4��Ѫ������鵰�����Լ��ٻ���ʧ������鵰�����ڸ����������Ѫ�쵰��ϵ����ǵ��ף�����ֵΪ0.7-1.5g/L(70-150mg/dl)��Ѫ���ں�Ѫ������Ѫ����鵰���������͡��ڸ�Ⱦ����֢������������Ƥ����̴�����ʱ�������ࡣ��ˣ��ڽ��ͽ��ʱ�뿼���������ص�Ӱ�졣
������5��Ѫ������Ѫ�쵰��Ũ�����ߡ�����Ѫ��������������Ѫ�쵰�ף�һ������������50mg/L(5mg/dl)��������Ѫ������Ѫʱ��Ѫ������Ѫ�쵰��Ũ�����߿ɴ�2.0g/L(200mg/dl)��Ѫ�����и���Ѫ����״���ʱ��Ѫ����ɽ��ɫ����ɫ�����÷ֹ��ȼƻ�Ѫ���Ӿ֤������ڡ���Ѫ������Ѫ������ѪҺ�д��ڵ�ʱ��Ϊ��Сʱ�����졣
������6�����ڳ���Ѫ�쵰�ף�������Ѫ������Ѫ���أ�������Ѫ����
������7����ϸ������ʱ�����̣���ϸ��������ʱ������Ѫ�����ز�ͬ���в�ͬ�̶ȵ����̣����÷����Ը���51Cr�����Բⶨ��������ϸ����T1/2(51Cr)Ϊ25��32�죬��ֵ����������ʾ��ϸ��������ʱ�����̣�Ҳ��ʾ��Ѫ���ࡣ���ڷ����Ժ��ؼ���ļ��������������㣬�۲�ʱ���ֳ������ٴ�������Ӧ�ý��٣�������ڿ��й�����
����2.���������������֤�ݡ�
������1����֯��ϸ�����ࡣ������Ѫ��ƶѪ��Ҫ֤��֮һ����֯��ϸ��������5��20����������Ѫ�߿ɸߴ�50��70�����ϣ����ڷ�������Σ��ʱ����֯��ϸ�����ɼ��ͻ���ʧ��
������2��ĩ��Ѫ�г����к˺�ϸ����������һ�㲻�ࡣ���ɼ����ȶ�ɫ�Ժ��ȼ��Ե�ʺ�ϸ������ϸ����С���Ⱥ����ν����ԡ��ɼ������Ρ����Ρ����Ρ����λ������ϸ����ѪС��Ͱ�ϸ������������������࣬����ijЩ��Ѫ��ƶѪʱҲ���Լ��١����Դ�����Ѫ���������Ѫ����Ӧ��
������3����������ϸ�������������࣬��������½����á�������������Ҷ��ȱ�����ɳ��������ϸ��������Ҷ�����ƺ���ʧ������������ֵ�������ϰ�Σ��ʱ������ϵϸ���������١�
����������ȷ��������һ����Ѫ��ƶѪ���ɸ�����Ҫѡ�������������顣
����1����ϸ����̬�۲졡�����ϸ����̬�ı��Ϊ��Ѫ��ƶѪ����ṩ��Ҫ�������������κ�ϸ�����࣬�����Ŵ������κ�ϸ������֢����������Ѫ��ƶѪ������ϸ����ʾ���к�ƶѪ��Ѫ�쵰��E����Ѫ�쵰��C���ȣ�����ϸ��������ϸ������ʾ��е����Ѫ��ƶѪ������ϸ������ʾ����ϸ����ƶѪ�������������ࡣ
����2����ϸ���������顡�Ƿ�ӳ��ϸ������������ݻ�������ϵ��һ�ּ��鷽�������ϸ������������ݻ�������С����������ӣ�������������Լ��ͣ������������Ŵ�������ϸ������֢����ϸ�����Լ��ͼ��ڰ��κ�ϸ��֢��
����3�����������飨Coombs���飩���ⶨ����������ȫ�Ŀ��塣ֱ�ӿ����������Dzⶨ���ߺ�ϸ���������Ų���ȫ���壬��ӿ����������Dzⶨ����Ѫ����������ȫ���壬�������������ԣ���ʾ����������Ѫ��ƶѪ���ɽ�һ������Ѫ��ѧ�������ȷ��������ʣ��ڲ���ԭ���������ʣ�����ȫ���Ժ���Ǵ����ܰ������ȡ�
����4���ữѪ����Ѫ���飨Ham���飩���������ߺ�ϸ�������1/6N�����ͬ������Ѫ���ϡ�37�������з���1��2Сʱ�ɼ���Ѫ����Ϊ���ԣ����Խ����ʾ����˯����Ѫ�쵰������ˮ��Ѫ����Ҳ��Ϊ�������˯����Ѫ�쵰����֮��ɸ���顣
����5������Ѫ�쵰��ԭ���顡��������Ѫ�쵰��ԭ�ʣ�75����G��6PDȱ��ʱ��ԭ�ʽ��͡����⣬ӫ������顢����Ѫ�ᣭ�軯�����鼰�������鵰��С�������������Խ��Ҳ��ʾG6PDȱ����G6PDȱ�������Ե�������Ҫø��������ϸ����Ѫ������G6PD��NADP�������Էֹ��ȼ�340nm�ⶨNADP����NADPH�Ļ�ԭ�ʡ�
����6������Ѫ���顡��Ѫ�ܱ�ATP���������������Ǿ�����ʾ��ͪ�ἤøȱ����
����7����������鼰�����ȱ������顡���Խ����ʾ���ȶ�Ѫ�쵰�ס�
����8��Ѫ�쵰��Ӿ�Ϳ���Ѫ�쵰�����顡������ϵ��к�������Ѫ�쵰�ײ���ͨ��Ѫ�쵰��Ӿ�ֱ�ijЩѪ�쵰���京����HbA��������Hb��Ҫ�ɷ֣�ռ95����HbA2����������3����������������������HbF�Լ�����Һ�ĵֿ�������������Ѫ�쵰�ߣ��ڼ�����Һ������һ��ʱ�����������Ѫ�쵰�ɱ��Ի��������HbF����Ӱ�죬�Դ˿ɼ��HbF����С��2����
��������
������Ѫ��ƶѪ��һ�������ʲ�ͬ�ļ����������Ʒ�������һ�Ŷ��ۡ��ܵ�����ԭ�����£�
����һ���������ơ�
����ȥ�����������Ϊ��Ҫ�������Ϳ���������������Ѫ��ƶѪӦע�������ů���϶�������Ӧ����ʳ�ò϶��;��������ʵ�ҩ�ҩ���������Ѫ��Ӧ����ͣҩ����Ⱦ�������Ѫ��Ӧ���������Ⱦ���ƣ��̷������������ߣ�Ҫ��������ԭ������
����������Ƥ�ʼ��غ������������Ƽ���
����������������Ѫ��ƶѪ��������ͬ��������Ѫ��������˯����Ѫ�쵰����ȣ�ÿ��ǿ����40��60mg���ִοڷ������⻯������ÿ��200��300mg�����Σ�������������Ѫ��ƶѪ���û����������������ʻ������Danazol���ȡ�
��������Ƣ�г�����
����Ƣ�г���Ӧ֤�����Ŵ������κ�ϸ������֢Ƣ�г���������Ч��������������Ѫ��ƶѪӦ����Ƥ�ʼ���������Чʱ���ɿ���Ƣ�г������۵��к�ƶѪ��Ƣ���ܿ����߿���Ƣ�г�������������Ѫ��ƶѪ�����ͪ�ἤøȱ�������ȶ�Ѫ�쵰�ײ��ȣ���ɿ�����Ƣ�г�������Ч�����϶���
�����ġ���Ѫ��
����ƶѪ����ʱ����Ѫ����Ҫ�Ʒ�֮һ������ijЩ��Ѫ����£�Ҳ����һ����Σ���ԣ������������������Ѫ��ƶѪ������Ѫ�ɷ�����Ѫ��Ӧ����PNH������ѪҲ���շ���Ѫ��������Ѫ�������ƹ�����������Ѫ����,����Ӧ��������Ѫ������Ѫ��Ҫ�ߣ����ֻ���ϸ������������ˮϴ�����κ�ĺ�ϸ����һ������£����ܿ�����Ѫ���ɽ�������Ѫ���ܾ���ƶѪ��
�����塢������
��������Ҷ��ȱ���ߣ��ڷ�Ҷ���Ƽ���������Ѫ�쵰�����ȱ��������Ӧ����������PNH���˲�������ʱӦ����������������ʹPNH���˷���������Ѫ��
���Ʋ�����