第九章 肿瘤与遗传
在人们生活的环境中存着不少物理的、化学的和生物的致癌因子,它们在一定条件下可以诱发肿瘤。例如,各种电离辐射和紫外线照射可以引起白血病和皮肤癌;多环芳烃化合物如3,4-苯并芘可以引起肺癌,黄曲霉素可以诱发肝癌;亚硝受可以引起各种消化道肿瘤;在生物因子中,已经证明某些病毒可以引起动物肿瘤,并与一些人类肿瘤如鼻咽癌、白血病密切有关。这些因子是通过引起基因异常而致瘤的。
但是尽管人们都接触各种致癌因子,却远非人人都发生肿瘤,这表明还存在个体的易感性,而易感性在很大程度是遗传物质的结构或功能才能使正常细胞转变为癌细胞,但对不同肿瘤,环境因素只有改变遗传因素作用的大小各异。
近年来肿瘤的分子遗传学研究表明,一些与细胞的生长和分化有关的基因在癌变过程中起关键作用,这些基因称为癌基因和肿瘤抑制基因,它们的结构或功能异常使细胞得以无控制生长,并最终导致肿瘤发生。
因此,有人认为,肿瘤是一种遗传病,可称为体细胞遗传病,因在其发生发中基因及基因异常起着重要作用。已知一些肿瘤是按照孟德尔方式遗传的,而在另一些肿瘤中遗传的“易感基因”和环境因素共同发挥作用;还有一些肿瘤是由于特定基因发生体细胞突变引起的,这种突变虽然不是遗传得来的,但却发生在遗传物质。
道德列举一些事实说明肿瘤发生中的遗传因素,然后再介绍瘤细胞的染色体和基因异常以及肿瘤发生的遗传机理。
第一节 肿瘤发生中的遗传因素
一、肿瘤的家族聚集现象
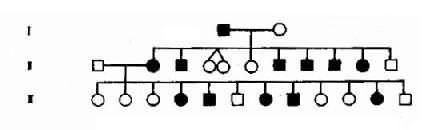
1.癌家族 癌家族(cancer family)是指一个家系中恶性肿瘤的发病率高(约20%),发病年龄较早,通常按常染色体显性方式遗传,以及某些肿瘤(如腺癌)发病率很高等。Lynch将上述特点归纳为“癌家族综合征”。曾经报告过一个癌家族(G家族,图9-1),经地70多年(1895年开始)间的五次调查,有些支系已传至第七代,在842名后裔中共发现95名癌患者,其中患结肠腺癌(48人)和子宫内膜腺癌(18人)者占多数。这95人中有13人肿瘤为多发性,19人癌发生于40岁之前;95名患者中72人有双亲之一患癌,男性与女性各47和48人,接近1:1,符合常染色体显性遗传。

图9-1 癌家族G部分系谱图
2.家族性癌 家族性癌(familial carcinoma)是指一个家族内多个成员患同一类型的肿瘤,例如,12%-25%的结肠癌患者有肠癌家族史。许多常见肿瘤(如乳腺癌、肠癌、胃癌等)通常是散发的,但一部分患者有明显的家族史。此外,患者的一级亲属中发病率通常高于一般人群3-4倍。这类癌的遗传方式虽然还不很清楚,但表明一些肿瘤家族聚集现象,或家族成员对这些肿瘤的易感性增高。
再者,在对77对患白血病的双生子调查中发现,同卵双生者发病一致率非常高;在另一调查中,20对同卵双生子均患同一部位的同样肿瘤。这些都说明遗传因素在肿瘤发病中的作用。
二、肿瘤发病率的种族差异
某些肿瘤的发病率在不同种族中有显著差异。如在新加破的中国人、马来人和印度人鼻咽癌发病率的比例为13.3:3:0.4.移居到美国的华人鼻咽癌的发病率也比美国白人高34倍。其它一些肿瘤类似情况。如黑人很少患Ewing骨瘤、睾丸癌、皮肤癌;日本妇女患乳腺癌比白人少,但松果体瘤却比其它民族多10余倍。种族差异主要是遗传差异,这也证明肿瘤发病中遗传因素起着重要作用。
三、遗传性肿瘤
一些肿瘤是按孟德尔方式遗传的,亦即由单个基因的异常决定的。它们通常以常染色体显性方式遗传,并有不同程度的恶变倾向,故也称为遗传性癌前改变。现举例如下。
1.家族性结肠息肉 家族性结肠息肉(familial polyposis coli,FPC)又称为家族性腺瘤样息肉症,在人群中的发病率为1:100000。表现为青少年时结肠和直肠已有多发性息肉,其中一些早晚将恶变。90%未经治疗的患者将死于结肠癌。FPC的基因现定位于5q21.
2.Ⅰ型神经纤维瘤Ⅰ型神经纤维瘤(neurofibromatosis,NF1)患者沿躯干的外周神经有多发的神经纤维瘤,皮肤上则可见多个浅棕色的“牛奶咖啡斑”,腋窝有广泛的雀斑,在少数患者肿瘤还有恶变倾向。现知与NF1发生密切有关的是一个肿瘤抑制基因,称为NF1基因,它定位于17q11.2,并已分离克隆。
此外,基底细胞痣综合征(basal cell nevus syndrome)、恶性黑素瘤(malignant melanoma)等属于遗传性肿瘤。
还有一些肿瘤既有遗传的,也有散发的。前者临床上按常染色体显性方式遗传,属遗传型,常为双侧性或多发性,发病早于散发型病例。这些肿瘤大多来源于神经或胚胎组织,虽然比较罕见,但在肿瘤病因研究中具有重要意义,故择要介绍如下。
1.视网膜母细胞瘤 视网膜母细胞瘤(retinoblastoma),为眼球视网膜的恶性肿瘤,多见于幼儿,大部分患者(70%)2岁前就诊,发病率为1:15000-28000。肿瘤的恶性程度很高,可随血循环转移,也能直接侵入颅内(图9-2)。
视网膜母细胞瘤可分为遗传型和散发型。大约40%的病例属遗传型,即由于父母患病或携带有突变基因,或父母的生殖细胞发生突变,在患儿出生时全身细胞已有一次视网膜母细胞瘤基因(Rb1)的突变。另约60%则是患者本人Rb1基因两次体细胞突变的结果,属非遗传型。遗传型患者常为双侧或多发肿瘤,平均发病年龄也较散发型者为早(15个月:30个月)。双侧性患者中还有少数患者可见一条13号染色体异常,主要是其长臂1区4带的缺失。13号长臂的这一区带正是视网膜母细胞瘤基因所在之处。
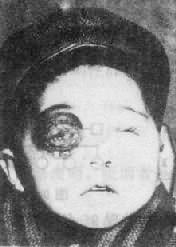
图9-2 双侧视网膜母细胞瘤右眼已萎缩
2.神经母细胞瘤 神经母细胞瘤(neuroblastoma)也是一种常见于儿童的恶性胚胎瘤,起源于神经嵴,活婴中的发病率为1:10000。神经母细胞瘤为常染色体显性遗传性肿瘤。有的神经母细胞瘤还合并有来源于神经嵴的其他肿瘤,如多发性神经纤维瘤、节神经瘤、嗜铬细胞瘤等。
3.Wilms瘤 Wilms瘤即肾母细胞瘤(nephr oblastoma),是一种婴幼儿肾的恶性胚胎性肿瘤,约占全部肾肿瘤6%,活婴中的发病率约为1:10000,3/4的肿瘤均在4岁以前发病。也可分为遗传型(38%)和非遗传型(62%),前者双侧性肿瘤较多,发病年龄较早,呈常染色体显性遗传,有明显的家族聚集现象。患者可伴有无虹膜症、半侧肥大、假两性畸形以及智力低下等。
一些易患Wilms瘤的无虹膜症患者有11号染色体短臂1区(11p13)缺失,而在Wilms瘤细胞中也曾发现11p13的缺失。现在认为11p13和11p15上有2个与肿瘤有关的基因,它们的异常都可能与Wilms瘤的发生有关。
四、染色体不稳定综合征
有一些隐性遗传病患者除易患肿瘤外,同时还有全身染色体容易断裂或对紫外线特别敏感的特点,这表明肿瘤与染色体不稳定之间有某种联系,这一类疾病称为染色体不稳定综合征,现择要介绍几种。
1.Fanconi贫血 Fanconi贫血(Fanconi’s anemia)是一种儿童期的骨髓疾病,表现为全血细胞减少,故又称为先天性血细胞减少症(congential pancytopenia)。患者有贫血、易疲乏、易出血和感染等症状,并常伴有先天畸形,尤其是大拇指或桡骨发育不良(或缺如),以及皮肤色素沉着等。患者的染色体自发断裂率明显增高,单体断裂、裂隙等染色单体畸变很多,双着丝粒体、断片、核内复制也很常见(图9-3)。约10%患者转变为白血病(主要是粒单型),且死于白血病者比正常人群高约20倍。
2.Bloom综合征 Bloom综合征(Bloom’s syndrome)多见于东欧犹太人的后裔。患者身材矮小,对日光敏感,故面部常有微血管扩张性红斑。患者外周血培养细胞有各种类型的染色体畸变和单体畸变,包括许多对称的四射体,姐妹染色单体交换率也比正常人高10倍。本病患者易患肿瘤或白血病。

图9-3 Fanconi贫血的异常染色体a示单位断裂;b示非同源染色体断裂后交换
3.毛细血管扩张性共济失调 毛细血管扩张性共济失调(ataxia telangiectasia,AT)为一种多见于儿童期的染色体隐性遗传病。1岁左右即可发病,表现为小脑性共济失调;6岁后眼和面、颈部出现瘤样小血管扩张。由于常有免疫缺陷,患者常死于感染性疾病。AT患者也有较多的染色体断裂。染色体畸变是非随机的,但常见有14/14易位或其它涉及14号染色体的改变。此外,B、D及G组的染色体重排也比较常见。患者的细胞对X线也特别敏感,其DNA修复能力明显下降。AT患者易患各种肿瘤,在45岁之前其患肿瘤的人数比正常人群增加3倍,主要是淋巴细胞白血病、淋巴瘤、网织细胞肉瘤等。人群中大约有1%AT的杂合子,他们占45岁以前死于肿瘤患者的5%。
4.着色性干皮病 着色性干皮病(xeroderma pigmentosum)患者皮肤对紫外线特别敏感,易出现多个的皮疹和色素沉着(图9-4)。患者染色体自发断裂率虽然没有增高。但在紫外线照射后明显上升,细胞也很容易死亡,存活下来的细胞由于DNA修复酶的缺陷而不能正常修复,常导致血管瘤、基底细胞癌等肿瘤发生。
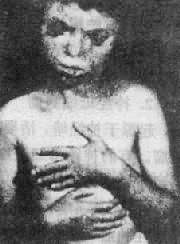
图9-4 着色性干皮病患者
五、肿瘤的遗传易感性
以上列举的许多事实都说明肿瘤发病中遗传因素的存在,因此肿瘤可以认为是基因染色体异常引起的疾病,其中一些遗传性肿瘤按照经典的孟德尔方式传递,但在更多情况下遗传的只是肿瘤的易感性,即易感基因,在个体易感染状态下如再发生体细胞突变,突变细胞就容易转化为肿瘤细胞。
个体的肿瘤遗传易感性是由特定的基因-染色体组合决定的。虽然对这些“易感基因(predisposing genes)”及其如何发挥作用了解得还不很清楚,但有一些事例表明它们可能通过生化的、免疫的和细胞分裂的机制促进肿瘤发生。
1.酶活性异常酶活性的改变可以影响致癌化合物在体内的代谢和灭活,例如芳烃羟化酶(arylhydrocarbon hydroxylase,AHH)它能在体内活化许多致癌的多环芳烃,包括从吸烟获得的各种芳烃,从而促进癌的发生。这种酶的可诱导性在人群中呈多态性,并按常染色体显性遗传(参阅第八章);另一方面酶的缺乏也可以导致对肿瘤的易感状态,例如着色性干皮病患者易患皮肤癌,这是由于DNA修复酶的缺陷导致细胞恶性变。
2.遗传性免疫缺陷 机休正常的免疫监视(immuune surveillance)系统不仅能抵御外来抗原的侵入,同时也能识别成为“异已”的突变细胞并加以排斥,免疫缺陷能使突变细胞得以逃脱这种监视而发展成为肿瘤。许多免疫缺陷患者都有易患肿瘤的倾向,例如无丙球蛋白血症(Bruton型)患者易患白血病和淋巴系统肿瘤等。
3.染色体病 先天愚型患者急性白血病的发病率比正常人群高15-18倍。这两种疾病可能有共同的发病机制,即细胞分裂机制的紊乱。此外,Klinefelter综合征患者易患男性乳腺癌;一些两性畸形患者中(主要是表型女性而有XY核型者),由发育不全的性腺(睾丸的残留组织)也易发生精原细胞瘤和性母细胞瘤。
现今已知至少有200余种单基因决定的性状或疾病具有不同程度的易患肿瘤的倾向,这类疾病可称为遗传性癌前疾病。