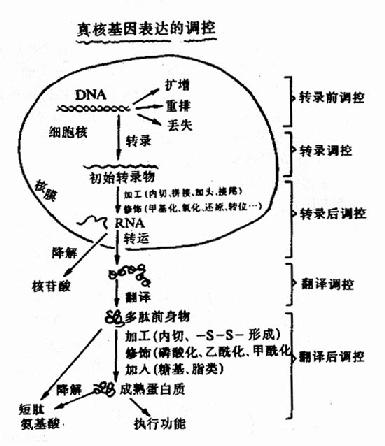
�����ڡ���˻���������
����һ����˻�����ĸ�����
������ԭ������Ƚϣ��������Ļ������Ϊ���ӣ����о����¡�
��������˻������ԭ�˻������ö࣬�˾�������Լ4��106bp���������������109bp����������ϸ����ǧ�����˾�Լ��4000����������Լ��10�������
���������������Ҫ���Ŵ��������鵰�ȹ���Ⱦɫ�ʣ��������ں�Ĥ�ڣ�������Ŵ��ɷ�(��������DNA��)����������˻��������صIJ�κ����ԡ�
������ԭ������Ļ�����������ǵ����壬����˻������Ƕ����塣
��������ǰ������ϸ��������������سɴ����У���ɲ���Ԫ�Ļ��������صĵ�Ԫ����ͬ������رգ�ת¼����˳����(polycistron)��mRNA�������������һ���ṹ����ת¼����һ��mRNA����mRNA�ǵ�˳����(monocistron)��������û�в���Ԫ�Ľṹ�������ϸ����������Ե���������ͬ�Ͳ�ͬ�Ķ����γɵ��ǻ����ɵģ�����漰���������Э����������⣬����������Э������Ҫ��ԭ�����︴�ӵöࡣ
������ԭ�˻�����Ĵ����ж�Ϊ������룬�������ӽ���ʵ�������������������н�Լ10%������Ϊ�����ʡ�rRNA��tRNA�ȱ��룬����Լ90%�����й������������
������ԭ������Ļ���Ϊ�����ʱ�������о�������������ģ����������Ϊ�����ʱ���Ļ����������Dz������ģ�����������(exon)���ں���(intron)��ת¼���辭����(splicing)ȥ���ں��ӣ����ܷ����������ĵ����ʣ���������˻��������صĻ��ڡ�
������ԭ�˻������г�rRNA��tRNA�����ж�������⣬�ظ����в��ࡣ���鶯�������������ڴ����ظ�����(repetitive sequences)���ø��Զ���ѧ��ʵ������������ظ����У��ٸ߶��ظ�����(highly repetitive sequences)����������һ��϶̣���10��300bp���ڲ�������������ظ�106�����ң�ռ������DNA����������10��60%���˵Ļ���������������Լռ20%�����ܻ������ˡ����ж��ظ�����(moderately repetitive sequences)���������ж�����100��500bp���ظ�101��105�Σ�ռ������10-40%�����粸�����к�������һ�ֳ�ΪAlu�����У���Լ300bp���ڲ����ͬ���������ƣ��ڻ��������ظ�3-��105�Σ����˵Ļ�������Լռ7%������Ҳ��������������˵Ļ�������18S/28SrRNA�����ظ�280�Σ�5SrRNA�����ظ�2000�Σ�tRNA�����ظ�1300�Σ�5���鵰�Ļ������ɴ��ظ�30-40�Σ���Щ���ɹ����ж��ظ����з�Χ���۵���������(single copy sequences)���������л����ϲ��ظ���ռ������������50-80%�����˻�������Լռ65%����������������Ϊ�����ʱ���Ļ����ڵ�����������ж����ظ����ǵ������Ļ���
�����������ɼ���˻������ԭ�˻����鸴�ӵö࣬�����������˻��������ʶ�������ޣ�ʹ���ڹ������ƶ����˻������о��ƻ�(human gene project)��ɣ������ȫ�������Ⱦɫ�嶨λͼ������˻�����109bpȫ��DNA���к�Ҫ�������ȫ������Ĺ��ܼ������ϵ���ر���Ҫ���˻��������ص�ȫ�����ɣ�����Ҫ�����ܳ��ڼ���о����̡�
����������˻��������ص��ص�
���������������ڶ���˻���������֪�������࣬����ԭ������Ƚ�������һЩ���Ե��ص㡣
����(һ)��˻��������صĻ��ڸ���
������ǰ��������������ǻ���ת¼�����롢������������Եĵ����ʵ��������̡�ͬԭ������һ����ת¼��Ȼ�����������������ص���Ҫ���ڡ�����˻���ת¼������ϸ����(����������ת¼����������)����������ڰ��������������Ƿֿ��ģ��������������˸���Ļ��ں����ԣ�ת¼��ĵ���ռ���˸���ķ�����ͼ19-13��Ҫ���г���˻������ĸ������ܵĻ��ڡ�

ͼ19��13�����������������صĿ��ܻ���
����ͼ19��13�ܽ�����ǰ�½��������Ļ��������̣�������һЩ�²��䡣ͼ�б�������ϸ���ڷֻ������лᷢ����������(gene rearrangement)������ԭ�Ի�������ijЩ���������ϱ仯�γɵڶ���������������������嵰�Ļ��������ܰ�ϸ���ֻ����������У���ԭ���ֿ��ļ��ٸ���ͬ�Ŀɱ�������ѡ����ϡ��仯����㶨������һ���ȶ��ġ�Ϊ�ض����������嵰�ױ���Ŀɱ���Ļ������ֻ�������ʹϸ���������ü��ٸ���������Ƭ�Σ���ϱ仯�������ܱ����108�ֲ�ͬ����Ļ������о��и��ӵĻ��������ػ�����
�������⣬���ϸ���л��ᷢ����������(gene amplification)�����������е��ض�������ijЩ����»Ḵ�Ʋ�������������緢�ֵ����ܵij�����ϸ�����ܾ���ķ�����������rRNA����(�ɳ�ΪrDNA)������2000�����Ժ��������������ϸ��Ҳ��ͬ��������������Ȼ�ʺ����ܾ���Ѹ�ٷ�������Ҫ�ϳɴ��������ʣ���Ҫ�д��������塣����MTX(methotrexate)��Ҷ��Ľṹ�����һЩ������ϸ����Ժ�������Ҷ��������Ķ���Ҷ�ỹԭø(dihydrofolate reductase, DHFR)�����DNA��������40?00����ʹDHFR�ı������������ӣ��Ӷ���߶�MTX�Ŀ��ԡ���������������ܹ���������������������������ֵ��ػ������������
����(��)��˻����ת¼��Ⱦɫ�ʵĽṹ�仯���
������˻�����DNA���ֶ���ϸ���������鵰�Ƚ�ϳ�Ⱦɫ�ʣ�Ⱦɫ�ʵĽṹ��Ⱦɫ����NA���鵰�Ľṹ״̬��Ӱ��ת¼����������������
����1.Ⱦɫ�ʽṹӰ�����ת¼��ϸ������ʱȾɫ��Ĵֵ�����ʱ�ɿ���ɢ�ں��ڣ���Ϊ��Ⱦɫ��(euchromatin)����ɢ��Ⱦɫ���еĻ������ת¼��Ⱦɫ���е�ijЩ���ε������ں����������ֽ����ɿ����Ա��ֽ����۵��Ľṹ���ڼ��ں��п��Կ�����Ũ���İ߿飬��Ϊ��Ⱦɫ��(heterochromatin)�����д�δ���л���ת¼���ԭ���ڳ�Ⱦɫ���б���Ļ������Ƶ���Ⱦɫ����Ҳ��ֹͣ������������ϸ��2��XȾɫ�壬������һ�������Ⱦɫ���ߣ�����XȾɫ���ϵĻ����ȫ��ʧ��ɼ����ܵ�Ⱦɫ�ʽṹ��ֹ������
����2.�鵰�����á���������ʵ��۲쵽�鵰����DNA�����ֹDNA�ϻ����ת¼��ȥ���鵰�������ܹ�ת¼���鵰���Ǽ��Ե����ʣ�������ɣ�����DNA���ϴ�����ɵ���������ϣ��Ӷ��ڱ���DNA���ӣ�������ת¼�����ܰ����˷�����������������ã�Ⱦɫ���еķ��鵰�׳ɷ־�����֯ϸ�������ԣ����������鵰��������������Ե�ȥ�����ת¼���á�
�������ֺ�С���һ���۲��С��ṹ�����ת¼�Ĺ�ϵ�����ֻ�Ծת¼��Ⱦɫ�����Σ��и�����������鵰��(H1�鵰��)ˮƽ���ͣ�H2A��H2B�鵰�����岻�ȶ������ӡ��鵰��������(acetylation)�ͷ��ػ�(ubiquitination)���Լ�H3�鵰���ϻ�����������Щ���Ǻ�С�岻�ȶ����������ػ�ָ����ת¼��Ծ������Ҳ��ȱ����С��Ľṹ����Щ��������С��ṹӰ�����ת¼��
����3.ת¼��Ծ����Ժ���ø�������ж����ӡ�Ⱦɫ��DNA��DNase ������ͨ���ᱻ�����00��400����bp��Ƭ�Σ���ӳ�������ĺ�С�������ظ��ṹ������Ծ����ת¼��Ⱦɫ��������DNase ������������100��200bp��DNAƬ�Σ��ҳ��̲���һ��˵����DNA���鵰���ڸǵĽṹ�б仯�������˶�DNase ������е�(hypersensitive site)�����ָ����е㳣������ת¼�����5�����(5��flanking region)��3��ĩ�˻��ڻ����ϣ����ڵ��ص����λ��ĸ����������������С��Ľṹ�����仯�����������ڵ��ص���϶��ٽ�ת¼��
����4.DNA���˽ṹ�仯����Ȼ˫��DNA�Ĺ������Ǹ��Գ��������������Ծת¼ʱ��RNA�ۺ�øת¼����ǰ��DNA�Ĺ��������Գ�������������DNAΪ���Գ����������Գ��������ɢ��С�壬������RNA�ۺ�ø��ǰ�ƶ�ת¼�������Գ������������ں�С������γɡ�
����5.DNA������α仯�����DNA�еİ����Լ��5%������Ϊ5���������(5��methylcytidine,m5C)������Ծת¼��DNA�����а���़����̶ȳ��ϵ͡����ּ����������ijЩ����5�������CpG�����У�ʵ�����������м�����ʹ���Ļ�����ת¼�����������谭ת¼������DNA�ض���λ�Ľ�ϴӶ�Ӱ��ת¼������û����еķ�����ȥ��Ҫ��DNA����ø��С�����̥�Ͳ��������������������ɼ�DNA�ļ����Ի�������������Ҫ�ġ�
�����ɴ˿ɼ���Ⱦɫ���еĻ���ת¼ǰ��Ҫ��һ��������Ĺ��̣���Ŀǰ�Լ�����ƻ�ȱ����ʶ��
����(��)��˻�����������Ե���Ϊ��
�������RNA�ۺ�ø�������ӵ������ܵͣ������ϲ�������������ʼת¼����Ҫ�������ּ����Эͬ���á���˻����������ȻҲ�����и��Ե���Ԫ����������ڲ����ձ飻��˻���ת¼����ĵ��ص���Ҳ��������ͼ������û�������������ߣ����ܵ����Լ��������Ϊ������������˻�����û�е��ص�������ʱ�Dz�ת¼�ģ���Ҫ����ʱ��Ҫ�м���ĵ��������ٽ�ת¼������֮����˻�����������Ե���Ϊ������
����������˻���ת¼ˮƽ�ĵ���
�������ϸ��������RNA�ۺ�ø(��͢�)�У�ֻ��RNA�ۺ�ø����ת¼����mRNA��������Ҫ����RNA�ۺ�ø���ת¼���ء�
����(һ)˳ʽ����Ԫ��(cis��acting elements)
������˻����˳ʽ����Ԫ���ǻ�����Χ��������ת¼���ӽ�϶�Ӱ��ת¼��DNA���С�������Ҫ�������Ե������õ�˳ʽ����Ԫ��������������(promoter)����ǿ��(enhancer)�������ַ������Ե������õ�Ԫ����������(silencer)��
����1.�����ӡ���ԭ�������ӵĺ�����ͬ����ָRNA�ۺ�ø��ϲ���ת¼��DNA���С������ͬ�����Ӽ䲻��ԭ�����������Թ�ͬһ�µ����У����ҵ���RNA�ۺ�ø���Խ��DNA����ת¼��������Ҫ���ֵ��������ӵ��Э�����ã���ͬ���������������벻ͬDNA��������ã���ͬ����ת¼��ʼ�����������ĵ�������Ҳ����ȫ��ͬ�������ͬ����������Ҳ�ܲ���ͬ��Ҫ��ԭ�˸����ӡ�����Ҳ���������������һ�����ת¼��ʼ�㼰������Լ100��200bp���У����������ɾ��ж������ܵ�DNA����Ԫ����ÿ��Ԫ��Լ��7��30bp������IJ�����RNA�ۺ�ø���������е�Ԫ�����м���19��1����
��19��1��������RNA�ۺ�ø���������г�����Ԫ����
| Ԫ������ | ��ͬ���� | ��ϵĵ������� | ||
| ���� | ������ | ���DNA���� | ||
| TATAbox | TATAAAA | TBP | 30,000 | ��10bp |
| GC box | GGGCGG | SP-1 | 105,000 | ��20bp |
| CAA box | GGCCAATCT | CTF/NF1 | 60,000 | ��22bp |
| Octamer | ATTTGCAT | Oct-1 | 76,000 | ��10bp |
| �� | �� | Oct-2 | 53,000 | ��20bp |
| kB | GGGACTTTCC | NFkB | 44,000 | ��10bp |
| ATF | GTGACGT | AFT | ? | 20bp |
�����������е�Ԫ�����Է�Ϊ���֣�
�����ٺ���������Ԫ��(core promoter element)��ָRNA�ۺ�ø��ʼת¼���������С��DNA���У�����ת¼��ʼ�㼰�����Σ�25/��30bp����TATA�С�����Ԫ������������ʱֻ��ȷ��ת¼��ʼλ��Ͳ�������ˮƽ��ת¼��
����������������Ԫ��(upstream promoter element)������ͨ��λ�ڣ�70bp������CAAT�к�GC�С��Լ���ת¼��ʼ���Զ������Ԫ������ЩԪ������Ӧ�ĵ������ӽ�������ı�ת¼Ч�ʡ���ͬ������в�ͬ������������Ԫ������λ��Ҳ����ͬ����ʹ�ò�ͬ�Ļ������ֱ��в�ͬ�ĵ��ء�ͼ19-14���˽�������Ϊ���ӣ�˵����˻�������������Ԫ������֯�����Ԫ����Ӧ��ϵ�ת¼���ӡ�
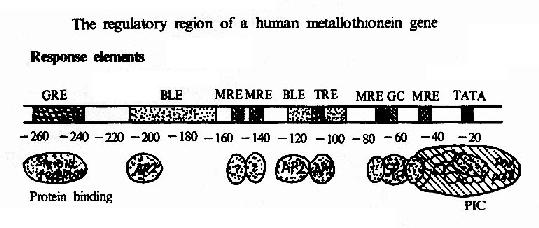
ͼ19��14���˽�������ĵ�����
����2.��ǿ�ӡ���һ���ܹ����ת¼Ч�ʵ�˳ʽ����Ԫ������������SV40�����з��ֵij�Լ200bp��һ��DNA����ʹ�Բ�Ļ���ת¼���100��������ڶ���������������ԭ�������ж���������ǿ�ӡ���ǿ��ͨ��ռ100��200bp���ȣ�Ҳ��������һ��������������ɣ��������������Ϊ8��12bp�����Ե���������������ʽ���ڡ���ǿ�ӵ������������ص㣺
��������ǿ�����ͬһ��DNA���ϻ���ת¼Ч�ʣ�����Զ�������ã�ͨ���ɾ���1��4kb������������뿪�����صĻ���30kb���ܷ������ã������ڻ�������λ����ζ��������á�
��������ǿ�������������е����������أ�����ǿ�ӷ�������Ȼ�������á����������ӵ��Ͳ��������ã��ɼ���ǿ�����������Ǻܲ���ͬ�ġ�
��������ǿ��Ҫ�������Ӳ��ܷ������ã�û�������Ӵ��ڣ���ǿ�Ӳ��ܱ��ֻ��ԡ�����ǿ�ӶԶ���û���ϸ��רһ�ԣ�ͬһ��ǿ�ӿ���Ӱ�첻ͬ���������ӵ�ת¼�����統������ǿ�ӵIJ�������������������ϸ��������ʱ���ܹ���ǿ��������������ijЩ�����ת¼������ǿ����ijЩȾɫ�������λʱ��Ҳ������Ƶ�����λ����Χ�����ת¼��ʹijЩ������ת¼������ǿ����������������������֮һ��
��������ǿ�ӵ����û�����Ȼ������ȷ����������˳ʽ����Ԫ��һ�����������ض��ĵ��������Ϻ���ܷ�����ǿת¼�����á���ǿ��һ�������֯��ϸ�������ԣ�������ǿ��ֻ��ijЩϸ������֯�б��ֻ��ԣ�������Щϸ������֯�о��е������Ե����������������ġ�
����3.�����ӡ������ڽ�ĸ�з��֣��Ժ���T�ܰ�ϸ����T��ԭ��������ת¼��������֤ʵ���ָ�����˳ʽԪ���Ĵ��ڡ�Ŀǰ�������ڻ���ת¼���ͻ�ر��������õ������о������࣬�������е����ӿ����������ӵ����ÿɲ������з����Ӱ�죬Ҳ��Զ���뷢�����ã����ɶ���Դ����ı��������á�
����(��)��ʽ��������(trans��acting factors)
�����Է�ʽ����Ӱ��ת¼�����ӿ�ͳ��Ϊת¼����(transcription factors, TF)��RNA�ۺ�ø��һ�ַ�ʽ������ת¼�ĵ������ӡ������ϸ����RNA�ۺ�øͨ�����ܵ�������ת¼���ã�����Ҫ������ת¼���ӹ�ͬЭ������RNA�ۺ�ø����Ӧ��ת¼���ӷֱ��ΪTF��TF��TF��TF���о���ࡣ��19-2�г���˻���ת¼��Ҫ������TF��
��19-2��RNA�ۺ�ø��Ļ���ת¼���Ӫ�
| ת¼���� | ��������kD) | ���� |
| TBP | 30 | ��TATA�� |
| TF��-B | 33 | �鵼RNA�ۺ�ø��Ľ�� |
| TF��-F | 30,74 | ����ø |
| TF��-E | 34,37 | ATPø |
| TF��-H | 62,89 | ����ø |
| TF��-A | 12,19,35 | �ȶ�TF��-D�Ľ�� |
| TF��-I | 120 | �ٽ�TF��-D�Ľ�� |
������ǰ��Ϊ��TATA�н�ϵĵ���������TF��D����������TF��Dʵ�ʰ�������ɷ֣���TATA�н�ϵĵ�����TBP(TATAbox binding protein)����Ψһ��ʶ��TATA�в������ϵ�ת¼���ӣ�������RNA�ۺ�øת¼ʱ����Ҫ�ģ�������ΪTBP�������(TBP��associated factors TAF)�����ٰ���8������TBP���ܽ�ϵ����ӡ�ת¼ǰ����TF��D��TATA�н�ϣ��̶�TF��B����C����TBP��DNA�������ϣ���N��������RNA�ۺ�ø���ͽ�ϣ������������ǻ���ɵ�TF��F����װ�䣬TF��F����RNA�ۺ�ø�γɸ����壬������������ATP����������DNA����ø���ԣ��ܽǰ����DNA˫��������ת¼�������������á����������������о���TF��D��B��F��RNA�ۺ�ø�����γ�һ��������ȡ�����ת¼���ܻ�����ת¼ǰ��ʼ������(pre��intitiation complex, PIC)����ת¼mRNA��TF��H�Ƕ��ǻ��������壬����������ATP����������DNA����ø���ԣ���ת¼�������з������ã�TF��E�������ǻ���ɵ��ľ��壬��ֱ����DNA��϶���������TF��B��ϵ�������ATPø�Ļ��ԣ�TF��E��TF��H�ļ�����γ�������ת¼������(ͼ19?5)����ת¼�������ɳ���RNA��TF��A���ȶ�TF��D��TATA�еĽ�ϣ����ת¼Ч�ʣ�������ת¼������һ����Ҫ�ġ�
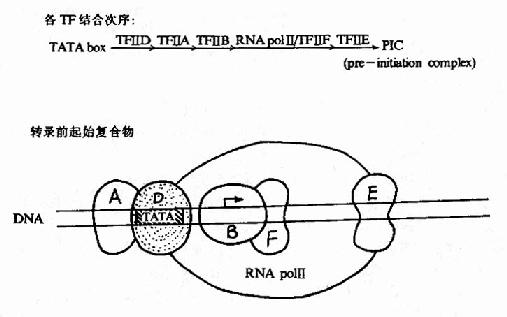
ͼ19-15��RNA�ۺ�ø��ת¼��������γ�ʾ��ͼ
�������������ǵ��͵���������ת¼��������γɣ����е���������Ӳ���TATA�л�ͨ��TATA�п�ʼת¼�������е���TATA�е��������ǿ�TF��I��TF��D��ͬ����ȶ���ת¼��ʼ�����忪ʼת¼�ġ��ɴ˿��Կ������ת¼��ʼ�ĸ����ԡ�
������ͬ�����ɲ�ͬ������������Ԫ����ɣ����벻ͬ��ת¼���ӽ�ϣ���Щת¼����ͨ���������ת¼���������ö�Ӱ��ת¼��Ч�ʡ������Ѿ����������ͬ��ת¼���ӣ������������ǣ�ͬһDNA���пɱ���ͬ�ĵ���������ʶ����ֱ�ӽ��DNA���еĵ�������������������ͬ�ĵ������Ӽ��������ã��������ת¼������ͨ�������ʣ������ʼ�������DNA������ϵ��Ӱ��ת¼Ч�ʵ�(��ͼ19��16)��ת¼����֮���ת¼������DNA�Ľ�϶���������ı仯���Ӷ�Ӱ��ת¼��Ч�ʡ�
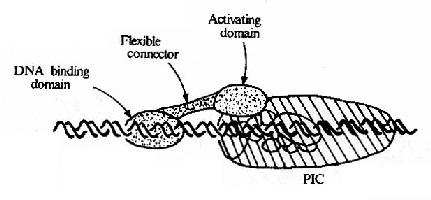
ͼ19-16��ת¼������ת¼�����������ģʽͼ
����ͼ19-��6��ʾ����Ϊ�����ʵ�ת¼���Ӵӹ����Ϸ�����ṹ�ɰ����в�ͬ����DNA�����(DNa binding domain)������60��100��������л���֯�ļ���������ɣ���ת¼������(activating domain)������30��100������л���ɣ���ṹ���и����������ᡢ�����Ȱ�����������������Ȳ�ͬ���࣬�����Խṹ�������������������������������ṹ��IJ��֡�����DNAֱ�ӽ�ϵ�ת¼����û��DNA�������ͨ��ת¼������ֱ�ӻ���������ת¼�������Ӱ��ת¼Ч�ʡ�
������DNA��ϵ�ת¼���Ӵ���Զ�������ʽ�����ã���DNA��ϵĹ����������¼��֣�
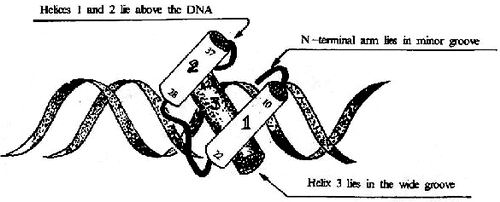
ͼ19��17��HTH�ṹ������DNA�Ľ��
������������ת�Ǫ�����(helix��turn��helix, HTH)������-��-����(helix��loop��helix,HLH)������ṹ����������������������ɶ��Ķ��γɵ�ת�ǻ����ӣ�����������motif�ṹ�Զ�������ʽ���������������൱��DNAһ���ݾ�(3.4nm)�������������պ÷ֱ�Ƕ��DNA���(ͼ19��17)��
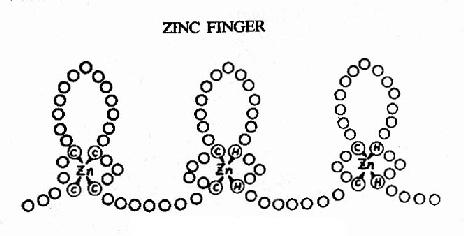
ͼ19��18�������ʵ�пָ�ṹ
������пָ(zinc finger)����ṹ��ͼ19��18��ʾ��ÿ���ظ��ġ�ָ��״�ṹԼ��23��������л���п��4����ۼ���4�����װ��ᡢ��2�����װ����2���鰱�����ϡ����������ʷ��ӿ���2?��������пָ�ظ���λ��ÿһ����λ������ָ������DNA˫����������Ӵ�5�������ᡣ������GC�н�ϵ�ת¼����SP1�о���������3��пָ�ظ��ṹ��
�������ۼ��ԣ�����������(basic leucine zipper, bZIP)���ýṹ���ص��ǵ����ʷ��ӵ�������ÿ��6�����������һ��������л�������͵�����Щ������л����ڦ�������ͬһ��������֡�������ͬ�ṹ������������л���������ˮ����ϳɶ����壬�ö��������һ�˵��Ķθ�����������л��������������DNA˫�������ϴ�����ɵ�������Ž�ϡ������γɶ��������DNA���ͽ�������Խ��͡��ڸ��ࡢС����Ƥ��֬��ϸ����ijЩ��ϸ�����г�ΪC/EBP�����һ���൰�����ܹ���CAAT�кͲ�����ǿ�ӽ�ϣ��������������γ�bZIP������ṹ��
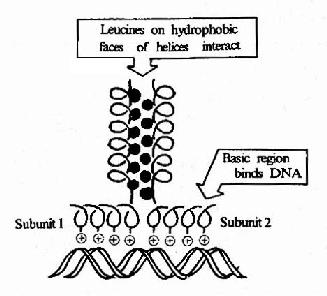
ͼ19��19�����������������ṹ������DNA�Ľ��
�����������ɼ���ת¼���ص�ʵ�����ڵ�������DNA���������뵰����֮�������ã�����ı仯���ǵ����ʺͺ��ᡰ��ı��֡������������Ӽ�ı��ϡ�����á��ṹ�ϵı仯������������е����壬���ǵ���ʶ���о���ֻ���Σ�������������������Ҫ�Ĺ������ǿ�������һ����֪���д���Ŭ��̽������
�� �¡��� Ҫ
������������ǻ���һϵ�в�����ֳ������﹦�ܵ��������̣����������ܡ���ȷ���صġ������麬�����������桢��������ͷ�ֳ����Ҫ��ȫ���Ŵ���Ϣ������Щ�Ŵ���Ϣ����ͬʱȫ���������������ͬ����֯ϸ����ϸ���ֻ�������ͬʱ�ڣ��������������ǿ�ȸ�����ͬ��������ϸ������̬���ܣ�����������Ӧ�����仯�ı������Ļ�������������棬�������������Ҳ����������֮���ڡ�ijЩ������ﲻ���ܻ���Ӱ�죬��Ϊ����Ա������ijЩ������������ϸ�����������������������ж�������Ҫ���ز����ٵģ���������Ϊ���һ�����һ�����������滷���źŶ��仯����Ϊ��Ӧ�Ա�������仯��ʹ�������ˮƽ����߳�Ϊ�յ���ʹ�������ˮƽ�����߳�Ϊ�����
�������������ؿ����ڸ��ơ����������ת¼��ת¼����ͷ����ȶ༶ˮƽ���У���mRNAת¼��ʼ�ǻ��������صĻ������Ƶ㡣ת¼��ʼ���ص�ʵ����DNA��������/�����ʪ������ʼ������ö�RNA�ۺ�ø���Ե�Ӱ�졣���ؽ��ʹ�������ˮƽ��ߵij�Ϊ���Ե���(�ϵ�)��ʹ�������ˮƽ������Ϊ���Ե���(�µ�)����ͬһ��������������ػ���������õĺ������г�Ϊ˳ʽ����Ԫ�����ܶԲ�ͬ�������ϵĻ��������������õĵ����ʳƷ�ʽ�������ӻ�ת¼���ӡ��������ϵ�˳ʽ����Ԫ���뷴ʽ���õ�����������ö����ػ�����
��������ԭ������Ļ���������Դ������й�ͬ���һ��ת¼���ص�λ������Ԫ����һ�������IJ���Ԫ��1ac����Ԫ������Ԫ����������Ԫ���У��ܵ��صĽṹ����Ⱥ�������ӡ������ӡ����ػ������ֹ�ӡ��еIJ���Ԫ������˥���ӡ���ͬһ�����ӿ����£��ӽṹ����Ⱥת¼�ϳɶ�˳����mRNA��ʵ��Э������ɵ��ػ������ϳɵĵ��ص��������ڲ��������У����������������õij�������ף���ٽ����������Ϊ����ס����ص������ض���С�������÷����乹���ı���Բ����ӵ����ã���������ԭ�˻�����Ӧ������仯���ı����ˮƽ�Ļ������ڡ�
������˻������ԭ�˴�ö࣬�ṹ�����ӣ����������ظ����У�������Ĵ����в���Ϊ�����ʱ���ģ���Ϊ�����ʱ���Ļ����������Dz������ġ��������������Dz�ȡ���������ر������ʽ����˻��������صĻ��ڸ��࣬ת¼ǰ�����л�������������ţ����漰Ⱦɫ�ʽṹ�ĸı䡢������̡�ת¼����صķ�ʽҲ�ܶ࣬������ת¼��ʼ����Ϊ�������Ե�������˻�����ص��������棬RNA�ۺ�ø��ת¼���������ڻ���ת¼���ӣ���ת¼ǰ���γ�ת¼�����壬��ת¼Ч�������൰�����ӵ�Ӱ�죬Э�������Ϊ���ӡ�Ŀǰ����˻��������ص���ʶ���о���ֻ���ڳ����Ρ���
��ϰ˼����
����1.ʲô�ǻ������?�����������仯���ص㼰����ض����������Ҫ�ԡ�
����2.Ϊʲô˵ת¼��ʼ�ĵ����ǻ��������ص����Ļ���?
����3.��ʵ������˵������Ԫ�����Ԫ���������ã�������������IJ���Ԫ�Ϳ��յ��IJ���Ԫ�ĵ��ط�ʽ��
����4.�Ƚ���˺�ԭ������Ļ������ͻ������������ƺͲ�֮ͬ����
����5.���������ӡ���ǿ�Ӻ�ת¼���ӵĸ���ṹ�����ܼ������ϵ������
����(������)