第二节 血细胞及其功能
血细胞包括红细胞、白细胞和血小板三类细胞,它们均起源于造血干细胞。在个体发育过程中,造血器官有一个变迁的程序。在胚胎发育的早期,是在卵黄囊造血,从胚胎第二个月开始,由肝、脾造血;胚胎发育到第五个月以后,肝、脾的造血活动逐渐减少,骨髓开始造血并逐渐增强;到婴儿出生时,几乎完全依靠骨髓造血,但在造血需要增加时,肝、脾可再参与造血以补充骨髓功能的不足。因此,此时的骨髓外造血具有代偿作用。儿童到4岁以后,骨髓腔的增长速度已超过了造血组织增长的速度,脂肪细胞逐步填充多余的骨髓腔。到18岁左右,只有脊椎骨、肋骨、胸骨、颅骨和长骨近端骨骺处才有造血骨髓,但造血组织的总量已很充裕。成年人如果出现骨髓外造血,已无代偿的意义,而是造血功能紊乱的表现。
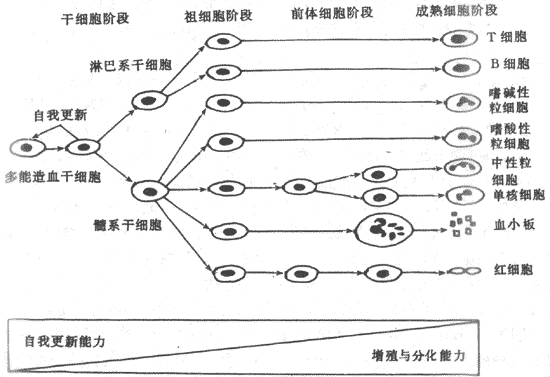
造血过程,也就是各类血细胞的发育、成熟的过程,是一个连续而又区分为阶段的过程。首先是造血干细胞(hemopietic stem cells)阶段,处于这一阶段的造血细胞为干细胞,它们既能通过自我复制(self renewal)以保持本身数量的稳定,又能分化形成各系定向祖细胞(committed progenitors);第二个阶段是定向祖细胞阶段,处于这个阶段的造血细胞,进一步分化方向已经限定,它们可以区分为:红系祖细胞,即红系集落形成细胞(CFU-E),粒-单核系祖细胞(CFU-GM),巨核系祖细胞( CFU-MK)和 TB淋巴系祖细胞(CFU-TB);第三个阶段是形态可辩认的前体细胞(precursors)阶段,此时的造血细胞已经发育成为形态上可以辨认的各系幼稚细胞,这些细胞进一步分别成熟为具有特殊细胞功能的各类终末血细胞,然后释放进入血液循环。造血细胞在经历上述发育成熟过程中,细胞自我复制的能力逐渐降低,而分化、增殖的能力逐渐增强,细胞数量逐步增大(图3-1)

图3-1造血细胞发育模式图
一、红细胞生理
1.红细胞的数量、形态和功能 红细胞(erythuocyte)是血液中数量最多的一种血细胞,正常男性每微升血液中平均约500万个(5.0×1012/L),女性较少,平均约420万个(4.2×1012/L).红细胞含有血红蛋白,因而使血液呈红色.红细胞在血液的气体运输中有极重要的作用.在血液中由红细胞运输的氧约为溶解于血浆的70倍;在红细胞参与下,血浆运输二氧化碳的能力约为直接溶解于血浆的18倍(详见第五章第三节).正常红细胞呈双凹圆碟形,平均直径约8μm,周边稍厚.这种细胞开头的表面积与体积之比,较球形时为大,因而气体可通过的面积也较大;由细胞中心到大部分表面的距离较短,因此气体进出红细胞的扩散距离也较短.这种形状也有利于红细胞的可塑性变形.红细胞在全身血管中循环运行,常要挤过口径比它小的毛细血管和血窦间隙,这时红细胞将发生卷曲变形,在通过后又恢复原状,这种变形称为塑性变形.表面积与体积的比值愈大,变形能力愈大,故双凹圆碟形红细胞的变形能力远大于异常情况下可能出现的球形红细胞.红细胞保持双凹圆碟形需要消耗能量。
红细胞膜是以脂质双分子层为骨架的半透膜。氧和二氧化碳等脂溶性气体可以自由通过,尿素也可以自由透入。在电解质中,负离子(如CI-、HCO3-)一般较易通过红细胞膜,而正离子却很难通过。红细胞内Na+ 浓度远低于细胞外,而细胞内K+浓度远高于细胞外,这种细胞内外的Na+、K+浓度差主要是依靠细胞膜上Na+泵的活动来维持的。低温贮存较久的血液,血浆内K+浓度升高,就是由于低温下代谢几乎停止,Na+泵不能活动的缘故。
红细胞结合和携带氧的过程并不消耗能量,血红蛋白中的Fe2+也不被氧化,若Fe2+被氧化成Fe3+成为高铁血红蛋白,即失去携氧能力。红细胞消耗葡萄糖,主要是通过糖酵解和磷酸戊糖旁路,所产生的能量(以结合于ATP的形式)主要是用于供应细胞膜上Na+泵的活动,用于保持低铁血红蛋白不致被氧化,也用于保持红细胞膜的完整性和细胞的双凹圆碟形。
2.红细胞比容红细胞在血液中所占的容积百分比,称为红细胞比容(hematocritvalue),可以用分血计(hematocrit)来测定。通常是将一定量的血液与抗凝剂混匀,置于用直径2.5mm的平底玻璃管制成的分血计中,以每分钟3000转的速度离心半小时,使血细胞下沉压紧,即可测出红细胞比容。正常成年人的红细胞比容,男性为40%-50%,女性为37%-48%。但这是从手臂等处浅静脉抽血测定的数值,并且这时在压紧的红细胞之间有很少量血浆;同时,全身各类血管中,血液的红细胞比容值也不尽相同。
3.正常红细胞生成所必需的原料和其它因素在幼红细胞的发育成熟过程中,细胞核的存在对于细胞分裂和合成血红蛋白有着重要的作用。在这些阶段,合成细胞核的主要构成物质—DNA必须有维生素B12和叶酸作为辅酶。
维生素B12是含钴的有机化合物,多存在于动物性食品中。机体对维生素B12的吸收必须要有内因子(intrinsic factor)和R结合蛋白(Rprotein)参与。内因子是由胃腺的壁细胞所分泌的一种糖蛋白,分子量在50000-60000之间,而R(rapid)蛋白是一种电泳速度很快的血浆蛋白。在酸性的胃液中,维生素B12主要与R蛋白结合,到了小肠上段处胰蛋白酶将这种结合断裂,维生素B12转而与内因子结合。内因子有两个活性部位,一个部位可与维生素B12结合,另一个部位则可与回肠上皮细胞膜上的特异受体结合。在正常情况下,内因子-B12复合物在小肠上段可保护维生素B12不受小肠内蛋白水解酶的破坏。当复合物运行至回肠段,便与回肠粘膜受体结合而被吸收进入门脉系统血流,一部分贮存在肝,一部分又与运输维生素B12的转钴蛋白Ⅱ(transcobalamineⅡ)结合,沿血液输送到造血组织,参与红细胞生成过程。当胃的大部分被切除或胃腺细胞受损伤,机体缺乏内因子,或体内产生抗内因子的抗体时,即可发生维生素B12吸收障碍,影响幼红细胞的分裂和血红蛋白合成,出现巨幼红细胞性贫血,即大细胞性贫血。
叶酸是以蝶酰单谷氨酸的形式吸收的。吸收之后,在双氢叶酸还原酶的催化下,形成四氢叶酸。存在于血浆中的叶酸几乎全是四氢叶酸的单谷氨酸盐。但进入组织细胞后,又通过酶促作用,再转变为多谷氨酸盐,才具有活性。叶酸缺乏时也引起与维生素B12缺乏时相似的巨幼红细胞性贫血。只是在维生素B12缺乏时,还可伴有神经系统和消化道症状。
合成血红蛋白还必须有铁作为原料,每亳升红细胞需要1mg铁,每天需要20-25mg铁用于红细胞生成,但人每天只需从食物中吸收1mg(约5%)以补充排泄的铁,其余95%均来自人体铁的再利用。机体贮存的铁主要来自于破坏了的红细胞。衰老的红细胞被巨噬细胞吞噬后,血红蛋白被消化而释出血红素中的Fe2+。这样释出的铁即与铁蛋白(ferritin)结合,此时的铁为Fe3+,聚集成铁黄素颗粒而沉淀于巨噬细胞内。血浆中有一种运铁蛋白(transferrin),可以来往运行于巨噬细胞与幼红细胞之间,以运送铁。贮存于铁蛋白中的Fe3+,先还原成Fe2+再脱离铁蛋白,而后与运铁蛋白结合。每分子运铁蛋白可以运送两个Fe2+,运送到幼红细胞后,又可反复作第二次运输。此外,还可以通过巨噬细胞与红母细胞直接接触,以提供合成血红蛋白所需的铁。由于慢性出血等原因,体内贮存的铁减少,或造血功能增强而供铁不够,均可引起小细胞性贫血,这主要是合成血红蛋白不足。此外,红细胞生成还需要氨基酸和蛋白质、维生素B6、B2、C、E,微量元素铜、锰、钴和锌等。
4.红细胞生成的调节 每个成年人体内约有25×1012个红细胞,每24小时便有0.8%的红细胞进行更新,也就是说每分钟约有160×106个红细胞生成;当机体有需要时,如失血或某些疾病使红细胞寿命缩短时,红细胞的生成率还能在正常基础上增加数倍。目前已经证明有两种调节因子分别调制着两个不同发育阶段红系祖细胞的生长。一种是早期的红系祖细胞,称为爆式红系集落形成单位(burst forming unit-erythroid,BFU-E),这是因为它们在体外培养中能形成很大的细胞集落,组成集落的细胞散布成物体爆炸的形状,这种早期祖细胞的生长和在体外形成集落都依赖于一种称为爆式促进因子(burst promoting activitor,BPA)的刺激作用。BPA是一类分子量为25000-40000的糖蛋白,以早期红系祖细胞BFU-E为作用的靶细胞,可能是促进更多的BFU-E从细胞周期中的静息状态(G0期)进入DNA合成期(S期),因而使早期祖细胞加强增殖活动。另一种是晚期的红系祖细胞,称为红系集落形成单位(colony forming unit-erythroid,CFU-E),它们在体外培养中只能形成较小的集落。晚期红系祖细胞对BPA不敏感,但主要接受促红细胞生成素(erythropoietin,EPO)的调节。促红细胞生成素是一种热稳定(80℃)的糖蛋白,分子量为34000。当组织中氧分压降低时,血浆中的促红细胞生成素的浓度增加,它促进红系祖细胞向前体细胞分化,又加速这些细胞的增殖,结果使骨髓中能合成血红蛋白的幼红细胞数增加,网织红细胞加速从骨髓释放。早在本世纪50年代,动物实验已显示了促红细胞生成素活性的存在,以后又确定促红细胞生成素主要由肾组织产生。切除双肾后,血浆中促红细胞生成素的浓度急剧降低。用分子生物学手段进一步证明,从肾组织细胞中已提取出编码促红细胞生成素的Mrna 和Cdna,还确定促红细胞生成素和mRNA和cDNA,还确定促红细胞生成素基因定位在7号染色体上。近年来有迹象提示人类的某些血液病,如再生障碍性贫血是红系祖细胞促红细胞生成素受体有缺陷所致(图3-2)。
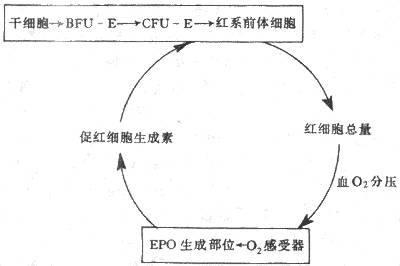
图3-2 EPOA调节红细胞生成的反馈调节环
促红细胞生成素主要由肾组织产生,但肾外,如肝脏,也有小量生成。晚期肾病患者,肾脏产生EPO已基本停止,但体内仍有小量EPO促使骨髓继续产生红细胞。
其他一些激素,包括雄激素、甲状腺激素和生长激素,都可增强促红细胞生成素的作用;雌激素则有抑制红细胞生成的作用。这可能是男性的红细胞数和血红蛋白量高于女性的原因。
二、白细胞生理
白细胞(leukocyte)是一类有核的血细胞。正常成年人白细胞总数是4000-10000/μ1,每日不同的时间和机体不同的功能状态下,白细胞在血液中的数目是有较大范围变化的。当每微升超过10000个白细胞时,称为白细胞增多,而每微升少于4000个白细胞时,称为白细胞减少。机体有炎症时常出现白细胞增多。
白细胞不是一个均一的细胞群,根据其形态、功能和来源部位可以分为三大类:粒细胞、单核细胞和淋巴细胞(表3-3)。白细胞与红细胞和血小板一样都起源于骨髓中的造血干细胞,在细胞发育过程中又都是经历定向祖细胞、前体细胞,而后成为具有各种细胞功能的成熟白细胞。
表3-3 血液中各类白细胞计数(细胞/μL)
| 均数 | % | 范围 | |
| 粒细胞 | |||
| 中性粒细胞 | 4150 | (59) | 1712~7588 |
| 嗜酸性粒细胞 | 165 | (2) | 0~397 |
| 嗜碱性粒细胞 | 44 | (<1) | 0~112 |
| 单核细胞 | 456 | (7) | 66~846 |
| 淋巴细胞 | 2185 | (31) | 1029~3341 |
| 白细胞 | 7000 | 2800~11200 |
引自Schmidt,R.F.&Thews,G,1989
白细胞的分化和增殖受到一组造血76生长因子(hematopoietic growth factor,HGF)的调节。这些因子从淋巴细胞、单核细胞和成纤维细胞生成并分泌,是一类糖蛋白。由于有些造血生长因子在体外可刺激造血细胞生成集落,故又称为集落刺激因子(clony stimulating factor, CSF)。目前从结构到功能已经充分阐明的集落刺激因子有M-CSF、G-CSF、GM-CSF、Multi-CSF、Meg-CSFt 和EPO等6种,除了EPO是调节红细胞生成因子之外,其余因子均参与调节白细胞的生成。这些因子中有的作用是广谱的,如Multi-CSF和GM-CSF(G是粒细胞缩写,M是单核细胞的缩写)的作用可以影响多系造血祖细胞的生成和发育,而其它一些因子(如G-CSF、M-CSF、GM-CSF)作用较为局限,只作用于某一系的造血祖细胞。所有这些因子除了作用于祖细胞,还能影响成熟白细胞的功能。此外,还有一类抑制性因子,如粒细胞抑素、乳铁蛋白和转化生成因子-β等,它们或是直接抑制白细胞的增殖、生长、或是限制上述的一些生长因子的释放或作用。
淋巴细胞的生成过程与其它白细胞有一些不同。在干细胞分化的早期,淋巴干细胞首先从多能干细胞分化出来。这些淋巴干细胞随血流进入初级(或中枢)淋巴器官,即骨髓和胸腺,在这里它们发育成定向淋巴细胞(commmittde lymphocyte)。在骨髓中发育的称为B细胞;在胸腺中发育的称为T细胞。随后,B和T细胞均随血流转移到二级(或外周)淋巴器官,即淋巴结和脾,在那里它们与某种抗原接触后即分化和增殖成为真正具有免疫功能的细胞,如浆细胞和T效应细胞(t effector cell)。淋巴细胞在生长成熟过程中接受一组称为白细胞介素(interleukins,ILs)的细胞因子的调节,T细胞在胸腺中还接受胸腺激素的作用(图3-3)。
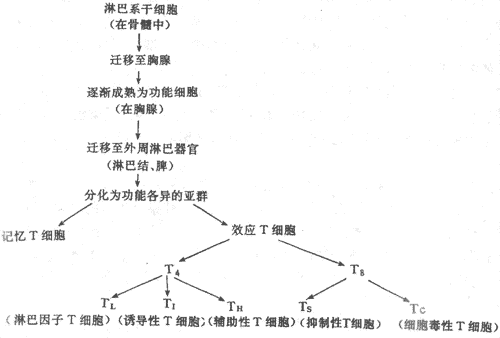
图3-3 T细胞的成熟和分化
所有的白细胞都能作变形运动,凭藉这种运动白细胞得以穿过血管壁,这一过程称作血细胞渗出(diapedisis)。白细胞具有趋向某些化学物质游走的特性,称为趋化性。体内具有趋化作用的物质包括:细菌毒素、细菌或人体细胞的降解产物,以及抗原-性体复合物等。白细胞按照这些物质的浓度梯度游走到这些物质的周围,把异物包围起来并吞入胞浆内,这称为吞噬作用。每类白细胞都具有某些酶类,如蛋白酶、多肽酶、淀粉酶、脂酶和脱氧核糖核酸酶等。在白细胞总数中,有一半以上存在于血管外的细胞间隙内,有30%以上贮存在骨髓内,其余的才是在血管中流动的。这些白细胞凭藉血液的运输,从它们生成的器官,即骨髓和淋巴组织,到达发挥作用的部位。
(一)粒细胞
约有60%的白细胞的胞质内具有颗粒,因而把它们称为粒细胞。又根据胞质中颗粒的染色性质不同将粒细胞区分为:中性、嗜酸性和嗜碱性粒细胞,这三类细胞的比例见表3-3。粒细胞在血流中停留时间很短暂,一般从数小时至2天。
1.中性粒细胞绝大部分的粒细胞属中性粒细胞。每微升血液中约有4500个中性粒细胞。由于这些细胞的细胞核的形态特殊,又称为多形核白细胞。中性粒细胞在血管内停留的时间平均只有6-8小时,它们很快穿过血管壁进入组织发挥作用,而且进入组织后不再返回血液中来。在血管中的中性粒细胞,约有一半随血流循环,通常作白细胞计数只反映了这部分中性粒细胞的情况;另一半则附着在小血管壁上。同时,在骨髓中尚贮备了约2.5×1012个成熟中性粒细胞,在机体需要时可立即动员大量这部分粒细胞进入循环血流。
中性粒细胞在血液的非特异性细胞免疫系统中起着十分重要的作用,它处于机体抵御微生物病原体,特别是在化脓性细菌入侵的第一线,当炎症发生时,它们被趋化性物质吸引到炎症部位。由于它们是藉糖酵解获得能量,因此在肿胀并血流不畅的缺氧情况下仍能够生存,它们在这里形成细胞毒存在破坏细菌和附近组织的细胞膜。由于中性粒细胞内含有大量溶酶体酶,因此能将吞噬入细胞内的细菌和组织碎片分解,这样,入侵的细菌被包围在一个局部,并消灭,防止病原微生物在体内扩散。当中性粒细胞本身解体时,释出各溶酶体酶类能溶解周围组织而形成脓肿。
中性粒细胞的细胞膜能释放出一种不饱和脂肪酸——花生四烯酸,在酶的作用下,由它再进一步生成一组旁分泌激素物质,如血栓素和前列腺素等,这类物质对调节血管口径和通透性有明显的作用,还能引起炎症反应和疼痛,并影响血液凝固(参看本章第三节及图3-8)。
2.嗜碱性粒细胞 在白细胞中嗜碱性细胞占0.5%-1%,即50个细胞/μ1。平均循环时间是12小时。这类粒细胞的胞质中存在较大和碱性染色很深的颗粒。颗粒内含有肝素和组织胺。近年来发现嗜碱性粒细胞参与体内的脂肪低谢。当食物中的脂肪被肠吸收后,周围血液中的嗜碱性粒细胞数随即增加。嗜碱性粒细胞释放出肝素(heparin),激活在血浆中的脂肪分解。这是由于肝素作为脂酶的辅基增强了脂酶的作用。结果加快了由脂肪分解为游离脂肪酸的过程。
嗜碱性粒细胞释放的组胺与某些异物(如花粉)引起过敏反应的症状有关(请参考免疫学教材)。
此外,嗜碱性粒细胞被激活时还释放一种称为嗜酸性粒细胞趋化因子A(eosinophile chemotactic factor A)的小肽,这种因子能把嗜酸性粒细胞吸引过来,聚集于局部以限制嗜碱性粒细胞在过敏反应中的作用。
3.嗜酸性粒细胞 血液中嗜酸性粒细胞占白细胞总数的2%-4%,即100-350个细胞/μ1。血液中嗜酸性粒细胞的数目有明显的昼夜周期性波动,清晨细胞数减少,午夜时细胞数增多。这种细胞数的周期性变化是与肾上腺皮质释放糖皮质激素量的昼夜波动有关的。当血液中皮质激素浓度增高时,嗜酸性粒细胞数减少;而当皮质激素浓度降低时,细胞数增加。嗜酸性粒细胞的胞质内含有较大的、椭圆形的嗜酸性颗粒。这类白细胞也具有吞噬功能。嗜酸性粒细胞在体内的作用是:①限制嗜碱性粒细胞在速发性过敏反应中的作用。当嗜碱性粒细胞被激活时,释放出趋化因子,使嗜酸性粒细胞聚集到同一局部,并从三个方面限制嗜碱性粒细胞的活性:一是嗜酸性粒细胞可产生前列腺素E使嗜碱性粒细胞合成释放生物活性物质的过程受到抑制;二是嗜酸性粒细胞可吞噬嗜碱性粒细胞所排出的颗粒,使其中含有生物活性物质不能发挥作用;三是嗜酸性粒细胞能释放组胺酶等酶类,破坏嗜碱性粒细胞所释放的组胺等活性物质。②参与对蠕虫的免疫反应。在对蠕虫的免疫反应中,嗜酸性粒细胞有重要的作用。这类粒细胞的细胞膜上分布有免疫球蛋白Fc片断和补体C3的受体。在已经对这种蠕虫具有免疫性的动物体内,产生了特异性的免疫球蛋白IgE。蠕虫经过特异性IgE和C3的调理作用后,嗜酸性粒细胞可借助于细胞表现的Fc受体和C3受体粘着于蠕虫上,并且利用细胞溶酶体内所含的过多氧化物酶等酶类损伤蠕虫体。在有寄生虫感染、过敏反应等情况时,常伴有嗜酸性粒细胞增多。
(二)单核细胞
第二类白细胞称为单核细胞,胞体较大,直径约为15-30酶μm,胞质内没有颗粒,它们约占血液中白细胞数的4%-8%。单核细胞来源于骨髓中的造血干细胞,并在骨髓中发育。当它们从骨髓进入血流时仍然是尚未成熟的细胞。与其他血细胞比较,单核细胞内含有更多的非特异性脂酶,并且具有更强的吞噬作用。单核细胞在血液中停留2-3天后迁移到周围组织中,细胞体积继续增大,直径可达50-80μm,细胞内所含的溶酶体颗粒和线粒体的数目也增多,成为成熟的细胞。固定在组织中的单核细胞称为组织巨噬细胞,它们经常大量存在于淋巴结、肺泡壁、骨髓、肝和脾等器官。激活了的单核细胞和组织巨噬细胞能生成并释放多种细胞毒、干扰素和白细胞介素,参与机体防卫机制,还产生一些能促进内皮细胞和平滑肌细胞生长的因子。在炎症周围单核细胞能进行细胞分裂,并包围异物。
(三)淋巴细胞
淋巴细胞是免疫细胞中的一大类,它们在免疫应答过程中起着核心作用。根据细胞成长发育的过程和功能的不同,淋巴细胞分成T细胞和B细胞两类。在功能上T细胞主要与细胞免疫有关,B细胞则主要与体液免疫有关。
1.T细胞 在血液的淋巴细胞中,约占70%-80%,在血液和淋巴组织之间反复循环,还可以停留在外周淋巴器官如淋巴结中。淋巴细胞的寿命较长,一般为数月,有的长达一年以上。T细胞被特异性的抗原物质激活后,进行增殖和分化,形成在功能上各异的两类细胞,即T免疫效应细胞T记忆细胞(t memory cell)。
根据T效应细胞的细胞表面特征的不同可区分为T4和T8两个亚群,而这些亚群还可根据不同的功能再分为不同类型。属于T4亚群的有:淋巴因子T细胞(t lymphokine cell,TL)、诱导性T细胞(T inductor cells,T1)和辅助性T细胞(t helper cells, TH)。淋巴因子T细胞能通过释放淋巴因子激活巨噬细胞和造血干细胞;T诱导性细胞能释放白细胞介素-2(interlukin-2),促进其他T细胞的成熟分化,而辅助性T细胞能产生一种B细胞生长因子(b cell growth factor),促使B细胞分化为浆细胞,影响抗体的产生。
T8亚型细胞,根据其功能可以再分为能抑制B细胞和T细胞活性的抑制性T细胞(t suppressor cells,Ts),和对带有特异抗原的靶细胞具有杀伤作用的细胞毒性T细胞(t cytotoxic cells, Tc)。由此可见,T细胞除了具有细胞免疫作用外,它们还具有调节其他免疫细胞特别是B细胞的功能。
长寿命的记忆T细胞在血液中不断循环,当他们再次遇到曾经接触过的抗原时,即使相隔几年之久仍能加以“识别”。在第二次与抗原体接触时能激发一种继发反应,这种反应比原发反应更强烈的引起细胞增殖,在短时间内形成大量的效应T细胞。T细胞各亚群的关系见图3-3。
2.B细胞 在血液中B细胞约占淋巴细胞总数的15%。固定在B细胞膜表面的免疫球蛋白(主要是单体IgM和IgD)是抗原的特异性受体。当它们初次与某一个抗原接触而被致敏时,一部分B细胞即分化成熟为浆细胞,浆细胞即开始生成对该抗原特异的免疫球蛋白并将它们释放到周围的组织液中,这就是免疫抗体。只有当某些调节性因子,如由辅助性T细胞所释放的淋巴因子和巨噬细胞释放的白细胞介素-1存在时,B细胞才能被抗原激活。浆细胞不再在血液中循环,在它们生存的2-3天时间里一直停留在组织中。
有小部分受抗原刺激的B细胞发展成为记忆性B细胞,寿命很长,且保持特异性,由它们增殖生成的后代细胞也保持着这种特异性。当它们再次接触具有同样特异性的抗原时,便能迅速被激活,成为特异B淋巴母细胞。由记忆性B细胞增殖生成的后代细胞愈多,被特异性抗原、激活的B细胞数也愈多。可见B细胞系统的“记忆”能力是取决于具有抗原特异性的记忆细胞数目的多少。
在血液中,除了T细胞和B细胞之外还有一类淋巴细胞,根据它们的细胞表面标志既不归属于B细胞,也不归属于T细胞。这类细胞称为裸细胞(null cell),约占血液中淋巴细胞总数的5%-10%。目前受注意的裸细胞有杀伤细胞(killer cell,K细胞)和自然杀伤细胞(matiral killer cell,NK细胞),K细胞上具有免疫球蛋白IgG的Fc片段受体,当表面覆盖有IgG(抗体)的靶细胞与K细胞接触时,IgG分子的Fc片段可与K细胞表面的Fc受体结合,激发K细胞的杀伤作用。由此可见,K细胞的杀伤作用是抗原依赖性的,但抗原是非特异的。至于NK细胞,虽然也是杀伤细胞,但其杀伤作用不依赖于抗原和抗体的存在。NK细胞广泛分布在血液和外周淋巴器官,对杀伤肿瘤细胞有重要作用。干扰素能活化NK细胞,而白细胞介素-2能刺激NK细胞的增殖和产生干扰素,因而增强NK细胞的杀伤作用。
三、血小板生理
血小板(platelets, thrombocyte)是从骨髓成熟的巨核细胞胞浆解脱落下来的小块胞质。巨核细胞虽然在骨髓的造血细胞中为数最少,仅占骨髓有核细胞总数的0.05%,但其产生的血小板却对机体的止血功能极为重要。每个巨核细胞均可产生1000-6000个血小板。
正常成年人的血小板数量是150000-350000个/μ/(150-350×109/L)。血小板有维护血管壁完整性的功能。当血小板数减少到50000个/μl(50×109/L)以下时,微小创伤或仅血压增高也使皮肤和粘膜下出现血瘀点,甚至出现大块紫癜。可能由于血小板能随时沉着于血管壁以填充内皮细胞脱落留下的空隙;而且,用同位素标记血小板示踪和电子显微镜观察,发现血小板可以融合入血管内皮细胞,因而可能对保持内皮细胞完整或对内皮细胞修复有重要作用。当血小板太少时,这些功能就难以完成而产生出血倾向。
循环血液中的血小板一般处于“静止”状态。但当血管受损伤时,通过表面接触和某些凝血因子的作用,血小板转入激活状态。激活了的血小板能释放一系列对止血过程必需的物质,关于血小板在止血过程中的作用可参看本章第三节。
生成血小板的巨核细胞也是从骨髓中的造血干细胞分化发展来的。造血干细胞首先分化生成巨核系祖细胞,也称巨核系集落形成单位(colony forming unit-megakaryocyte,CFU-Meg)。祖细胞阶段的细胞核内的染色体一般是2-3倍体。当祖细胞是2倍体或4倍体时,细胞具有增殖能力,因此这是巨核细胞系增加细胞数量的阶段。当巨核系祖细胞进一步分化为8-32倍体的巨核细胞时,胞质开始分化,内膜系统逐渐完备。最后有一种膜性物质把巨核细胞的胞质分隔成许多小区。当每个小区被完全隔开时即成为血小板,一个个血小板通过静脉窦窦壁内皮间的空隙从巨核细胞脱落,进入血流。
巨核细胞增殖、分化的调节机制类似于红细胞系生成的调节,至少受两种调节因子分别对两个分化阶段进行调节。这两种调节因子是:巨核系集落刺激因子(Meg-CSF)和促血小板生成素(thrombopoietin,TPO)。
巨核系集落刺激因子是主要作用于祖细胞阶段的调节因子,它的作用是调节巨核系祖细胞的增殖。骨髓中巨核细胞总数减少时促使该调节因子的生成增加,Meg-CSF是一种低分子糖蛋白,分子量约为46000,它与促血小板生成素具有完全不同的免疫学性质。
促血小板生成素也是一种糖蛋白,当血流中血小板减少时,促血小板生成素在血液中的浓度即增加。该调节因子的作用包括:①增强祖细胞的DNA合成和增加细胞多倍体的倍数;②刺激巨核细胞合成蛋白质;③增加巨核细胞的总数,结果增加了血小板的生成。根据去肾大鼠出现血小板减少时血液中促血小板生成素的浓度不增加的事实,推测肾是产生促血小板生成素的部位。
四、血细胞的破坏
血细胞常因衰老而被破坏,但也可因意外和各种病理原因而被破坏。破坏的方式各种血细胞不尽相同,这与各种细胞功能不同有关。
(一)红细胞的破坏
红细胞的平均寿命约为120天。在这期间,平均每个红细胞血管内循环流动约27km,在“旅途”中常常需要挤过去比它小的毛细血管及孔隙,因而不得不变形。当红细胞逐渐衰老时,细胞变形能力减退而脆性增加,在血流湍急处可因机械冲击而破损,在通过微小孔隙时也发生困难,因而特别容易停滞在脾和骨髓中被巨噬细胞所吞噬。事实上,任何组织都能使红细胞解体,这可从皮下出血的青紫块都会逐渐消失的事实证明。
红细胞在血管内破损而发生溶血,所释出的血红蛋白立即与一种血浆a2-球蛋白—触珠蛋白结合;但溶血严重达到每100m1血浆有100mg血红蛋白时,血浆中的触珠蛋白已不够用,未能与触珠蛋白结合的血红蛋白将经肾从尿中排出。与触珠蛋白结合的血红蛋白虽不致被排出,但将被肝摄取,脱铁血红素转变为胆色素,铁则以铁黄素的形式沉着于肝细胞内。在脾内被吞蚀的衰老红细胞,经消化后,铁可再利用,而脱铁血红素也转变为胆色素,运送到肝处理。
(二)血小板的破坏
血小板进入血液后,只在开始两天具有生理功能,但平均寿命可有7-14天。
在生理止血活动中,血小板聚集后本身将解体并释出全部活性物质;它也可能融入血管内皮细胞。这样看来,血小板除衰老破坏外,还可能在发挥其生理功能时被消耗。但是用51Cr或32P标记血小板观察其破坏的情况,发现血小板的破坏也随血小板的“日龄”而增多,即主要是衰老尔后被破坏。曾经对一些接受了抗凝处理的人进行观察,发现这时血凝过程虽被阻止,但血小板的寿命也不延长。这些事实,倾向于说明了平时的血管内凝血并不强(也可能这种凝血程度很小),不致影响全部血小板的平均寿命。衰老的血小板是在脾、肝和肺组织中被吞噬的。
白细胞的寿命较难准确判断。因为,粒细胞和单核细胞主要是在组织中发挥作用的;淋巴细胞则往返循环于血液-组织液-淋巴之间,而且尚可增殖分化。一般来说,中性粒细胞在循环血液中停留8小时左右即进入组织,一般三、四天后将衰老死亡;若有细菌入侵,粒细胞在吞噬活动中可释出溶酶体酶过多而发生“自我溶解”,与破坏的细菌和组织片共同构成脓。